Эукариотты ДНҚ репликациясы - Eukaryotic DNA replication - Wikipedia
Эукариотты ДНҚ репликациясы шектейтін механизм болып табылады ДНҚ репликациясы ұяшық циклына бір ретке дейін. Эукариотты ДНҚ репликациясы хромосомалық ДНҚ а-ны көбейту үшін орталық болып табылады ұяшық және эукариотты ұстау үшін қажет геном.
ДНҚ репликациясы - әрекеті ДНҚ-полимераздар бастапқы шаблон тізбегін толықтыратын ДНҚ тізбегін синтездеу. ДНҚ-ны синтездеу үшін екі тізбекті ДНҚ ДНҚ арқылы шешіледі геликаздар полимеразалардан озып, екі тізбекті шаблоннан тұратын репликациялық шанышқыны құрайды. Репликация процестері бір ДНҚ қос спиралын екі ДНҚ спиралына көшіруге мүмкіндік береді, олар еншілес жасушаларға бөлінеді митоз. Репликация шанышқысында жүзеге асырылатын негізгі ферментативті функциялар жақсы сақталған прокариоттар дейін эукариоттар, бірақ эукариоттық ДНҚ репликациясындағы репликация аппараты - бұл әлдеқайда үлкен кешен, репликация орнында көптеген ақуыздарды үйлестіріп, ауыстырады.[1]
Орындаушы толығымен көшіру үшін жауап береді геномдық Әр пролиферативті жасушадағы ДНҚ. Бұл процесс тұқым қуалайтын / генетикалық ақпараттың ата-ана жасушасынан еншілес жасушаға өтуіне мүмкіндік береді және осылайша барлық организмдер үшін өте қажет. Көп бөлігі жасушалық цикл ДНҚ репликациясының қатесіз жүруін қамтамасыз ету үшін салынған.[1]
Жылы G1 фаза жасуша циклінің көптеген ДНҚ репликациясының реттелетін процестері басталады. Эукариоттарда басым көпшілігі ДНҚ синтезі кезінде пайда болады S фазасы жасуша циклінің және бүкіл геномның екі қыз көшірмесін жасау үшін оралуы және қайталануы керек. Кезінде G2, кез келген зақымдалған ДНҚ немесе репликация қателері түзетіледі. Соңында, геномдардың бір данасы митозда немесе М фазада әр жасуша жасушасына бөлінеді.[2] Бұл қыздардың көшірмелерінде әрқайсысында ата-аналық дуплекстің бір тізбегі және жаңа туындайтын антипараллель тізбегі бар.
Бұл механизм прокариоттардан эукариоттарға дейін сақталған және белгілі жартылай консервативті ДНҚ репликациясы. ДНҚ репликациясының орны үшін жартылай консервативті репликация процесі - бұл ДНҚ спиралы ашық немесе жайылмаған, жұптаспаған ДНҚ-ны ашатын, шанышқы тәрізді ДНҚ құрылымы, репликациялық шанышқы. нуклеотидтер бос нуклеотидтерді қос тізбекті ДНҚ-ға енгізу үшін тану және негіздік жұптастыру үшін.[3]
Бастама
Эукариотты ДНҚ репликациясының басталуы - бұл ДНҚ синтезінің бірінші сатысы, мұнда ДНҚ қос спиралы оралмайды және жетекші тізбекте α ДНҚ полимеразасы пайда болады. Артта қалған оқиға реплика шанышқысын орнатады. ДНҚ спиралінің праймингі α ДНҚ полимеразасы арқылы ДНҚ синтезіне мүмкіндік беретін РНҚ праймерінің синтезінен тұрады. Өңдеу жетекші тізбектің басталуында және артта қалған жіпте әр Оказаки фрагментінің басында бір рет жүреді.
ДНҚ репликациясы деп аталатын белгілі бірізділіктен басталады репликацияның шығу тегі, және эукариотты жасушалар бірнеше репликациядан бастау алады. ДНҚ репликациясын бастау үшін бірнеше репликативті ақуыздар осы репликативті бастауларға жиналады және диссоциацияланады.[4] Төменде сипатталған жеке факторлар бірігіп қалыптасуына бағыт береді репликацияға дейінгі кешен (алдын-ала RC), репликацияны бастау процесінде негізгі аралық.
Қауымдастығы шығу тегі тану кешені (ORC) репликациядан басталады жасушалардың бөліну циклі 6 ақуыз Жүктеу платформасын құру үшін (Cdc6) минихромосомаларға қызмет көрсету (Mcm 2-7) кешені жеңілдетілген ақуыздар хроматинді лицензиялау және ДНҚ репликациясы факторы 1 ақуыз (Cdt1). ORC, Cdc6 және Cdt1 бірге Mcm2-7 кешенінің G байланысы кезінде репликативті шығуымен тұрақты байланысы үшін қажет.1 жасуша циклінің фазасы.[5]
Репликативті кешен
Репликацияның эвукариоттық бастаулары екі бағытты ДНҚ репликация шанышқыларының жиналуына әкелетін бірқатар ақуыз кешендерінің түзілуін бақылайды. Бұл іс-шаралардың бастамашысы репликацияға дейінгі кешен (алдын-ала RC) шағылыстыру бастауларында. Бұл процесс Г-да жүреді1 жасуша циклінің кезеңі. RC-ге дейінгі түзілу көптеген репликация факторларын, соның ішінде шығу тегі тану кешені (ORC), Cdc6 ақуызы, Cdt1 ақуызы және минихромосомаларға қызмет көрсететін ақуыздарды (Mcm2-7) біріктіруден тұрады.[6][7] Алдын ала RC пайда болғаннан кейін, кешеннің активтенуі екіден басталады киназалар, циклинге тәуелді киназа 2 (CDK) және Dbf4 тәуелді киназа (DDK), бұл ДНҚ-ның репликациясы басталғанға дейін инициациялық кешенге дейінгі RC-ге көшуге көмектеседі. Бұл ауысу ДНҚ-ны босату және көптеген эукариотты ДНҚ полимеразаларын жайылмаған ДНҚ айналасында жинақтау үшін қосымша репликация факторларының реттелген жиынтығын қамтиды. Репликация бастауларында екі бағытты реплика шанышқыларының қалай орнатылатыны туралы сұрақтың ортасында ORC репликацияға дейінгі кешенді құру үшін әрбір репликация шығу тегі үшін екі бастан Mcm2-7 комплекстерін шақыратын механизм болып табылады.[8][9][10]
Шығу тегін тану кешені
Репликацияға дейінгі кешенді (алдын-ала RC) құрастырудың алғашқы қадамы - байланыстыру шығу тегі тану кешені (ORC) репликацияның шығу тегі. Кеш митоз кезінде Cdc6 ақуызы байланысқан ORC-ге қосылады, содан кейін Cdt1-Mcm2-7 комплексімен байланысады.[11] ORC, Cdc6 және Cdt1 алты ақуыздың минихромосомаларын қолдау (Mcm 2-7) кешенін ДНҚ-ға жүктеу үшін қажет. ORC - бұл алты суббірлік, Orc1p-6, ақуыз кешені, ол репликацияны бастау үшін ДНҚ-да репликативті шығу орындарын таңдайды және хроматинмен байланысуы ORC клеткалық цикл арқылы реттеледі.[6][12] Әдетте, ORC суббірліктерінің функциясы мен мөлшері көптеген эукариоттық геномдарда сақталады, олардың айырмашылығы олардың әр түрлі ДНҚ-мен байланысатын орындарында.
Ең көп зерттелген шығу тегі тану кешені бұл Saccharomyces cerevisiae немесе байланыстыратыны белгілі ашытқы автономды түрде қайталанатын реттілік (ARS).[13] The S. cerevisiae ORC 30 аймақты қамти отырып, репликацияның ашытқы бастауының A және B1 элементтерімен ерекше әрекеттеседі. негізгі жұптар.[14] Осы реттіліктің байланысы қажет ATP.[6][14]
Атомдық құрылымы S. cerevisiae ARS ДНҚ-мен байланысқан ORC анықталды.[14] Orc1, Orc2, Orc3, Orc4 және Orc5 өзара әрекеттесудің екі түрінің көмегімен А элементін қоршап алады, негізі спецификалық емес және негіздік, А элементінде ДНҚ-ны бүгеді. Барлық бес суббірлік қант фосфат магистралімен А элементінің бірнеше нүктелерінде байланысып, негіз ерекшелігінсіз тығыз ұстаманы қалыптастырады. Orc1 және Orc2 A элементінің кіші ойығымен байланысады, ал Orc4 қанатты спираль домені кірістіру спиралы (IH) арқылы А элементінің негізгі ойығындағы инварианты Ц метил топтарымен байланысады. Метазоаналарда бұл IH болмауы[14] адамның ORC-дегі бірізділіктің жоқтығын ішінара түсіндіреді.[15] ARS ДНҚ-сы B1 элементінде Orc2, Orc5 және Orc6-мен өзара әрекеттесу арқылы бүгіледі.[14] ORC-тің шығу тегі ДНҚ-ны бүгуі эволюциялық жолмен сақталған сияқты, бұл Mcm2-7 күрделі жүктеме механизмі үшін қажет болуы мүмкін.[14][16]
ОРС репликация кезінде ДНҚ-мен байланысқан кезде, ол репликативті кешеннің басқа инициациялық факторларын құрастыру үшін тірек қызметін атқарады.[17] Бұл G-ді репликирлеуге дейінгі күрделі жиын1 жасуша циклінің кезеңі S фазасы кезінде ДНҚ репликациясының белсенуіне дейін қажет.[18] Хромосомадан комплекстің (Orc1) ең болмағанда бөлігін алып тастау метафаза метафаза аяқталғанға дейін репликативті комплекстің түзілуін болдырмауын қамтамасыз ету үшін сүтқоректілердің ОРК-нің бір бөлігі болып табылады.[19]
Cdc6 ақуызы
Байланыстыру жасушалардың бөліну циклі 6 (Cdc6) ақуыз шығу тегі тану кешеніне (ORC) репликация басталғанға дейінгі репликация кешенін (RC дейінгі) құрастырудың маңызды кезеңі болып табылады. Cdc6 ДНҚ-дағы ORC-мен ATP-тәуелділікте байланысады, бұл Orc1-ті қажет ететін түпнұсқа байланысу үлгісінің өзгеруін тудырады ATPase.[20] Cdc6 хроматинмен байланысуы үшін ORC қажет және Cdt1-Mcm2-7 гептамеріне қажет[11] хроматинмен байланысу үшін.[21] ORC-Cdc6 кешені сақина тәрізді құрылымды құрайды және басқа АТФ тәуелді ақуыз машиналарына ұқсас. Cdc6 деңгейлері мен белсенділігі репликация бастауларының жасушалық цикл кезінде қолданылатын жиілігін реттейді.
Cdt1 ақуызы
The хроматинді лицензиялау және ДНҚ репликациясы коэффициенті 1 (Cdt1) ақуыз ДНҚ репликациясы үшін хроматинді лицензиялау үшін қажет.[22][23] Жылы S. cerevisiae, Cdt1 Mcm2-7 жалғыз гексамерасының сол жақтағы ашық сақиналы құрылымын тұрақтандыру арқылы Mcm2-7 кешенін бір-бірден хромосомаға жүктеуді жеңілдетеді.[11][24][25] Cdt1-мен байланысатыны көрсетілген C терминалы Mcd ақуыздарының хроматинге ассоциациялануын ынталандыру үшін Cdc6.[26] OCCM (ORC-Cdc6-Cdt1-MCM) кешенінің крио-ЭМ құрылымы Cdt1-CTD Mcm6-WHD-мен өзара әрекеттесетінін көрсетеді.[27] Метазондарда жасуша циклі кезіндегі Cdt1 белсенділігі оның ақуызбен ассоциациялануымен қатаң реттеледі геминин, ол екеуі де ДНҚ-ның репликациясын болдырмау үшін S фазасында Cdt1 белсенділігін тежейді және оның алдын алады барлық жерде және одан кейінгі протеолиз.[28]
Минихромосомаларға қызмет көрсететін ақуыздар кешені
Минихромосомаларды қолдау (Mcm) ақуыздары ДНҚ репликациясының инициациялық мутанттары үшін генетикалық экранның атауымен аталды. S. cerevisiae ARS-ге тән тәсілмен плазмиданың тұрақтылығына әсер етеді.[29] Mcm2, Mcm3, Mcm4, Mcm5, Mcm6 және Mcm7 гексамерикалық кешен құрайды, ол Mcm2 мен Mcm5 арасындағы саңылауы бар ашық сақиналы құрылымға ие.[11] Mcm ақуыздарының хроматинге қосылуы шығу тегі тану кешенінің (ORC), Cdc6 және Cdt1 үйлесімді қызметін қажет етеді.[30] Mcm ақуыздары хроматинге салынғаннан кейін, ORC және Cdc6 хроматиннен кейіннен ДНҚ репликациясының алдын алмай шығарылуы мүмкін. Бұл байқау репликация алдындағы кешеннің негізгі рөлі Mcm ақуыздарын дұрыс жүктеу екенін көрсетеді.[31]

Хроматиннің құрамындағы Mcm ақуыздары екі сақинаның сәл қисайған, бұралған және центрден тыс екі гексамерді түзіп, орталық сақинада екі сақинаның шекарасында байланысқан ДНҚ түсірілген.[32][33] Әрбір гексамерикалық Mcm2-7 сақинасы алдымен репписоманы құрастыру үшін тірек қызметін атқарады, содан кейін репписоманың негізгі компоненті болып табылатын каталитикалық CMG (Cdc45-MCM-GINS) геликазасының өзегі ретінде қызмет етеді. Әрбір Mcm ақуызының басқалармен байланысы жоғары, бірақ суббірлік түрлерінің әрқайсысын ерекшелендіретін ерекше тізбектер эукариоттарда сақталған. Барлық эукариоттарда дәл алты Mcm протеині бар, олардың әрқайсысы қолданыстағы кластардың біріне жатады (Mcm2-7), бұл әрбір Mcm ақуызының ерекше және маңызды қызметі бар екенін көрсетеді.[34][9]
ДНҚ-геликазаның белсенділігі үшін минихромосомаларға қызмет көрсететін ақуыздар қажет. S фазасы кезінде алты Mcm ақуызының кез-келгенін активтендіру геликазаны қайта өңдеуге болмайды және оны репликация кезінде жинау керек деген репликация шанышқысының одан әрі өрбуіне жол бермейді.[35] Миникромосомаларды қолдау ақуыздар кешені геликаза белсенділігімен қатар, ATPase белсенділігімен де байланысты.[36] Mcm алты ақуызының кез-келгенінің мутациясы консервіленген ATP байланысатын орындарды азайтады, бұл ATP гидролизі Mcm кешенінің барлық алты бөлімшелерін қамтитын үйлестірілген оқиға екенін көрсетеді.[37] Зерттеулер көрсеткендей, Mcm ақуыздар кешенінде ATP гидролизін үйлестіру үшін бірге жұмыс жасайтын Mcm ақуыздарының ерекше каталитикалық жұптары бар. Мысалға, Mcm3 бірақ жоқ Mcm6 Mcm6 әрекетін белсендіре алады. Mcm2-7 кешендерінің крио-ЭМ құрылымдарымен расталған бұл зерттеулер,[11][32] Mcm кешені - бұл гексамер Mcm3 жанында Mcm7, Mcm2 жанында Mcm6, және Mcm4 жанында Mcm5. Каталитикалық жұптың екі мүшесі де АТФ-пен байланысуға және гидролизге мүмкіндік беретін конформацияға ықпал етеді және белсенді және белсенді емес суббірліктердің қоспасы Mcm ақуыз кешенінің ATP байланысуын және гидролизді толығымен аяқтауға мүмкіндік беретін үйлестірілген ATPase белсенділігін жасайды.[38]
The ядролық оқшаулау Минихромосомаларға қызмет ететін ақуыздар бүршігі бар жасушаларда реттеледі.[39][40] Mcm ақуыздары ядро G-да1 жасуша циклінің кезеңі мен S фазасы, бірақ экспортталады цитоплазма G кезінде2 сатысы және M фазасы. Жасуша ядросына ену үшін Mcm толық алты бүтін комплексі қажет.[41] Жылы S. cerevisiae, ядролық экспорт циклинге тәуелді киназа (CDK) белсенділігімен ықпал етеді. Хроматинмен байланысқан Mcm ақуыздары CDK-ге қол жетімділіктің болмауына байланысты CDK экспорттау техникасынан қорғалған.[42]
Бастама кешені
Г кезінде1 жасуша циклінің кезеңі, репликация инициациялық факторлары, шығу тегі тану кешені (ORC), Cdc6, Cdt1 және минихромосомаларға қызмет көрсету (Mcm) ақуыздар кешені, репликацияға дейінгі комплексті (RC-ге дейінгі) қалыптастыру үшін ДНҚ-мен дәйекті байланысады. Г-дің ауысуы кезінде1 жасуша циклінің S фазасына, S фазасына тән циклинге тәуелді ақуыз киназа (CDK) және Cdc7 / Dbf4 киназа (DDK) алдын-ала RC-ді белсенді реплика шанышқысына айналдырады. Бұл түрлендіру кезінде алдын-ала RC индукция кешенін құра отырып, Cdc6 жоғалуымен бөлшектеледі. Mcm ақуыздарының байланысуынан басқа, жасушалардың бөліну циклі 45 (Cdc45) ақуыз ДНҚ репликациясын бастау үшін өте қажет.[43][44] Зерттеулер көрсеткендей, Mcm хроматинге Cdc45-ті жүктеу үшін өте маңызды, ал құрамында Mcm және Cdc45 бар бұл кешен жасуша циклінің S фазасының басында пайда болады.[45][46] Cdc45 хроматинге жүктелген Mcm ақуыз кешенін G-ге дейін репликация басталғанға дейінгі RC құрамдас бөлігі ретінде бағытталған.1 жасуша циклінің кезеңі.[47]
Cdc45 ақуызы
Жасушалардың бөліну циклі 45 (Cdc45) ақуыз - репликативті комплексті инициациялық кешенге айналдыру үшін маңызды компонент. Cdc45 ақуызы репликация кезінде басталады және индикация басталуы үшін қажет Saccharomyces cerevisiaeжәне созылу кезінде маңызды рөл атқарады. Осылайша, Cdc45 хромосомалық ДНҚ репликациясының инициация және созылу фазаларында орталық рөлдерге ие.[48]
Cdc45 инициация басталғаннан кейін G соңында хроматинмен байланысады1 сатысы және жасуша циклінің S фазасы кезінде. Cdc45 физикалық түрде Mcm5-пен байланысады және Mcm гендер отбасының алты мүшесінің бесеуімен генетикалық өзара әрекеттесуді көрсетеді. ORC2 ген.[49][47] Cdc45-ті хроматинге жүктеу басқа репликация ақуыздарын, соның ішінде жүктеу үшін өте маңызды ДНҚ-полимераза α, ДНҚ-полимераза ε, репликация А ақуызы (RPA) және пролиферацияланатын жасушалық ядролық антиген (PCNA) хроматинге түседі.[46][50][51][52]Ішінде Ксенопус ядросыз жүйе, плазмидалық ДНҚ-ны босату үшін Cdc45 қажет екендігі дәлелденді.[52] The Ксенопус ядросыз жүйе сонымен қатар ДНҚ-ның ашылуы және РРА-ның хроматинмен тығыз байланысуы тек Cdc45 қатысуымен болатындығын көрсетеді.[46]
Cdc45-ті хроматинмен байланыстыру Clb-Cdc28 киназа белсенділігіне, сондай-ақ функционалды Cdc6 және Mcm2-ге байланысты, бұл Cdc45 S-фаза циклинге тәуелді киназалар (CDK) белсендірілгеннен кейін алдын-ала RC-мен байланысады. Уақыт пен CDK тәуелділігінде көрсетілгендей, Cdc45-ті хроматинмен байланыстыру ДНҚ репликациясын бастау үшін өте маңызды. S фазасында Cdc45 физикалық түрде хроматиндегі Mcm ақуыздарымен әрекеттеседі; алайда Cdc45-тің хроматиннен диссоциациясы Mcm-ге қарағанда баяу жүреді, бұл ақуыздардың әртүрлі механизмдермен бөлінетіндігін көрсетеді.[34]
ГИНС
Алты минихромосоманы ұстайтын ақуыздар мен Cdc45 репликация шанышқыларының қозғалуы және ДНҚ-ны босату үшін инициация және созылу кезінде өте қажет. GINS иницирлеу кезінде репликацияның бастауларында Mcm және Cdc45 өзара әрекеттесуі үшін, содан кейін репликом ілгерілегенде ДНҚ репликациясы шанышқыларында өте маңызды.[53][54] GINS кешені Sld5 (Cdc105), Psf1 (Cdc101), Psf2 (Cdc102) және Psf3 (Cdc103) төрт кішкентай ақуыздан тұрады, GINS «5, 1, 2, 3» дегенді білдіретін «go, ichi, ni, san» білдіреді. 'жапон тілінде.[55] Cdc45, Mcm2-7 және GINS бірге CMG геликазасын құрайды,[56] репликоманың репликативті геликазасы. Mcm2-7 кешенінің өзі геликаза белсенділігі әлсіз болғанымен [57] Cdc45 және GINS тұрақты helicase белсенділігі үшін қажет[58][59]
Mcm10
Mcm10 хромосомалардың репликациясы үшін өте маңызды және ДНҚ репликациясының бастауларында белсенді емес түрде жүктелетін минихромосомалардың 2-7 геликазасымен қызмет етеді. [60] [61] Mcm10 шаперондар каталитикалық ДНҚ-полимераза α және репликациялық шанышқылар кезінде полимеразаны тұрақтандыруға көмектеседі.[62][63]
DDK және CDK киназалары
S фазасының басталуында репликацияға дейінгі комплекс репликацияның басында инициациялық кешенді қалыптастыру үшін екі S фазаға тән киназалармен белсендірілуі керек. Бір киназа - Dbf4 тәуелді киназа (DDK) деп аталатын Cdc7-Dbf4 киназа, ал екіншісі циклинге тәуелді киназа (CDK).[64] Ашытқыдағы Cdc45 хроматинмен байланысатын талдау Ксенопус CDK әрекетінің төменгі ағыны жүктеме екенін көрсетті Ccc45 хроматинге.[44][45] CD6 Cdc6 мен CDK және CDK-ға тәуелді болғандықтан, CDK әрекетінің мақсаты болады деп болжанған фосфорлану Cdc6. C фазасына өту үшін Cdc6-нің CDK-тәуелді фосфорлануы қажет деп саналды.[65]
DDK, Cdc7 каталитикалық суббірліктері де, активатор ақуызы Dbf4 де эукариоттарда сақталады және жасуша циклінің S фазасының басталуына қажет.[66][67] DDK және Cdc7 екеуі де репликацияның хроматиндік бастауларына Cdc45 жүктеу үшін қажет. ДДК киназасын байланыстырудың мақсаты - Mcm кешені, мүмкін Mcm2.[68][66] ДДК Mcm кешенін мақсат етеді, ал оның фосфорлануы Mcm helicase белсенділігінің мүмкін активтенуіне әкеледі.[69]
Dpb11, Sld3 және Sld2 ақуыздары
Sld3, Sld2 және Dpb11 көптеген репликация белоктарымен әрекеттеседі. Sld3 және Cdc45 кешенді құрайды, олар G1-де репликацияның алғашқы бастауларында алдын-ала RC-мен байланысты1 фазасы және S фазасында репликацияның кейінірек пайда болуымен өзара Mcm тәуелділікте.[70][71] Dpb11 және Sld2 полимераза with-мен өзара әрекеттеседі және өзара байланыстыратын тәжірибелер Dpb11 және полимераза the S фазасында бір-біріне сіңіп, репликацияның бастауларымен байланысатындығын көрсетті.[72][73]
Sld3 және Sld2 CDK фосфорланған, бұл екі репликативті ақуыздың Dpb11-ге қосылуына мүмкіндік береді. Dpb11-де екі жұп BRCA1 C Terminus (BRCT) домендері болды, олар фосфопептидті байланыстыратын домендер ретінде белгілі.[74] BRCT домендерінің N-терминал жұбы фосфорланған Sld3-пен, ал C-терминал жұбы фосфорланған Sld2-мен байланысады. Бұл өзара әрекеттесулердің екеуі де ашытқыдағы ДНҚ бүршіктенетін ДНҚ-ны активтендіру үшін өте қажет.[75]
Dpb11 сонымен қатар GINS-пен өзара әрекеттеседі және ДНҚ-ның хромосомалық репликациясының инициациясы мен созылу кезеңдеріне қатысады.[54][76][77] ГИНС - репликация шанышқыларында кездесетін репликация ақуыздарының бірі және Cdc45 және Mcm-мен комплекс құрайды.
Бұл Dpb11, Sld2 және Sld3 арасындағы фосфорлануға тәуелді өзара әрекеттесулер ДНҚ репликациясының CDK-ға тәуелді активтенуі үшін өте маңызды және кейбір эксперименттер шеңберінде өзара байланыстыратын реактивтерді қолдану арқылы жүктеме алдындағы комплекс (алдын-ала LC) деп аталады . Бұл кешенде Pol ɛ, GINS, Sld2 және Dpb11 бар. Pre-LC CDK-ға тәуелді және DDK-ға тәуелді түрде шығу тегі бар кез-келген ассоциациядан бұрын пайда болады және CDK белсенділігі алдын-ала LC түзілуі арқылы ДНҚ репликациясының басталуын реттейді.[78]
Ұзарту

Репликативті кешеннің пайда болуы (алдын-ала РК) ДНҚ репликациясының басталуының мүмкін жерлерін белгілейді. Екі тізбекті ДНҚ-ны қоршап тұрған минихромосомаларды күту кешеніне сәйкес, алдын-ала RC түзілуі шығу тегі ДНҚ-ның дереу ашылуына немесе ДНҚ полимеразаларының қосылуына әкелмейді. Оның орнына G кезінде қалыптасатын алдын-ала RC1 жасуша циклінің жасушалары G-дан өткеннен кейін ғана ДНҚ-ны ашып, репликацияны бастау үшін белсендіріледі1 жасуша циклінің S фазасына дейін.[2]
Инициациялық кешен түзіліп, жасушалар S фазасына өткен соң, комплекс реписомаға айналады. Эукариотты респизомдық кешен ДНҚ репликациясын үйлестіруге жауап береді. Жетекші және артта қалған жіптерде репликацияны ДНҚ-полимераза ε және ДНҚ-полимераза by орындайды. Clascin, And1, репликация коэффициенті C қысқыш тиегіші және шанышқылардан қорғау кешені сияқты көптеген алмастырушы факторлар полимеразалық функцияларды реттеуге және шаблон тізбегін Cdc45-Mcm-GINS комплексімен ашумен үйлестіруге жауап береді. ДНҚ оралмаған кезде бұралу саны азаяды. Мұның орнын толтыру үшін жазу саны көбейеді, оңды енгізу супер орамалар ДНҚ-да. Егер бұл жойылмаса, ДНҚ репликациясы тоқтайды. Топоизомеразалар реплика ашасы алдында осы супер орамдарды алып тастауға жауапты.
Репписома әр пролиферативті жасушадағы бүкіл геномдық ДНҚ-ны көшіру үшін жауап береді. Негізгі спираль түзетін негіздік жұптасу және тізбектің түзілу реакциялары ДНҚ полимеразаларымен катализденеді.[79] Бұл ферменттер бір тізбекті ДНҚ бойымен қозғалады және шаблон тізбегін «оқып», оның құрамына кіретін ДНҚ тізбегін кеңейтуге мүмкіндік береді. пурин нуклеобазалар, аденин және гуанин, және пиримидин нуклеобазалар, тимин және цитозин. Тегін қосылды дезоксирибонуклеотидтер жасушада дезоксирибонуклеотид трифосфаттар (dNTPs) түрінде болады. Бұл бос нуклеотидтер соңғы енгізілген нуклеотидтің ашық 3'-гидроксил тобына қосылады. Бұл реакцияда бос дНТП-дан пирофосфат бөлініп, полимерлену реакциясы үшін энергия түзеді және 5 'монофосфатты шығарады, содан кейін 3' оттегімен ковалентті байланысады. Сонымен қатар, дұрыс енгізілмеген нуклеотидтерді жойып, орнына дұрыс энергетикалық реакция кезінде дұрыс нуклеотидтер қоюға болады. Бұл қасиет ДНҚ репликациясы кезінде пайда болатын қателерді дұрыс түзету және қалпына келтіру үшін өте маңызды.
Реплика ашасы
Репликациялық шанышқы - бұл жетекші және артта қалған жіптер деп аталатын жаңадан бөлінген шаблондық жіптер мен қос тізбекті ДНҚ арасындағы түйісу. Дуплексті ДНҚ антипараллель болғандықтан, ДНҚ репликациясы екі бағытта қарама-қарсы бағытта жүреді, репликация шанышқысындағы екі жаңа тізбек арасында, бірақ барлық ДНҚ полимеразалар ДНҚ-ны жаңадан синтезделген тізбекке қатысты 5-тен 3-ке дейін синтездейді. ДНҚ репликациясы кезінде одан әрі үйлестіру қажет. Екі репликативті полимераза ДНҚ-ны қарама-қарсы бағытта синтездейді. Полимераза DNA ДНҚ-ны «жетекші» ДНҚ тізбегінде синтездейді, өйткені ол репризомамен ДНҚ-ны босату бағытына бағытталады. Керісінше, полимераза δ ДНҚ-ны қарама-қарсы ДНҚ шаблон тізбегі болып табылатын «артта қалған» тізбекте бөлшектенген немесе үзілген түрде синтездейді.
Артта қалған ДНҚ репликациясының үзінділері Оказаки фрагменттері деп аталады және эукариоттық репликация шанышқысында ұзындығы шамамен 100-ден 200-ге дейін. Әдетте, артта қалған жіпте бір тізбекті байланыстыратын ақуыздармен қапталған бір тізбекті ДНҚ-ның ұзынырақ бөліктері бар, бұл екінші құрылымның пайда болуын болдырмай, бір тізбекті шаблондарды тұрақтандыруға көмектеседі. Эукариоттарда бұл бір тізбекті байланысатын ақуыздар ретінде белгілі гетеротримерлі кешен болып табылады репликация А ақуызы (RPA).[80]
Әрбір Оказаки фрагментінің алдында синтез кезінде келесі Оказаки фрагментінің жүруімен ығыстырылған РНҚ-праймер болады. RNase H РНҚ праймерлерін қолдану арқылы пайда болатын ДНҚ: РНҚ гибридтерін таниды және оларды праймер: шаблон түйінін қалдырып, қайталанатын тізбектен алып тастауға жауапты. ДНҚ-полимераза α, осы учаскелерді таниды және праймерді алып тастағаннан кейінгі үзілістерді созады. Эукариотты жасушаларда ДНҚ сегментінің аз бөлігі РНҚ праймерінің ағысына қарай ығыстырылып, қақпақша құрылымын жасайды. Содан кейін бұл қақпақ эндонуклеазалармен бөлінеді. Репликация шанышқысында қақпақты алып тастағаннан кейін ДНҚ-дағы саңылау тығыздалады ДНҚ лигазы I жаңадан синтезделген жіптің 3'-OH мен 5'фосфатының арасында қалған никтерді қалпына келтіреді.[81] Эукариоттық Оказаки фрагментінің салыстырмалы түрде қысқа болуының арқасында, артта қалған тізбекте үзіліссіз пайда болатын ДНҚ репликациясы синтезі жетекші тізбекті синтезге қарағанда аз тиімді және көп уақытты алады. Барлық РНҚ праймерін алып тастап, никтерді қалпына келтіргеннен кейін ДНҚ синтезі аяқталады.

Жетекші бағыт
ДНҚ-ны репликациялау кезінде реписом ата-аналық дуплексті ДНҚ-ны 5-тен 3 'бағытта екі бір тізбекті ДНҚ шаблонының репликация шанышқысына шығарады. Жетекші тізбек - репликация шанышқысының қозғалуымен бірдей бағытта қайталанатын шаблон тізбегі. Бұл жаңа синтезделген тізбекті бастапқы тізбектің комплементарымен 5 '-ден 3' дейін синтездеуге мүмкіндік береді, бұл репликация шанышқысының қозғалысы сияқты.[82]
Жетекші тізбектің 3 'ұшына примаза арқылы РНҚ праймерін қосқаннан кейін, жетекші тізбекке қатысты ДНҚ синтезі 3' тен 5 'бағытта үздіксіз жалғасады. ДНҚ-полимераза the шаблон тізбегіне нуклеотидтерді үздіксіз қосады, сондықтан жетекші синтездеу үшін тек бір праймер қажет және ДНҚ-полимеразаның үздіксіз белсенділігі бар.[83]
Артта қалу
Бойынша ДНҚ репликациясы артта қалған жіп үзілісті. Артта қалған тізбек синтезінде ДНҚ-полимераза репликация айырының қарама-қарсы бағытында бірнеше қолдануды қажет етеді РНҚ праймерлері. ДНҚ-полимераза деп аталатын ДНҚ-ның қысқа үзінділерін синтездейді Оказаки фрагменттері олар праймердің 3 'ұшына қосылады. Бұл фрагменттер эукариоттарда 100-400 нуклеотидтің арасында болуы мүмкін.[84]
Оказаки фрагменті синтезінің соңында ДНҚ-полимераза O алдыңғы Оказаки фрагментіне түсіп, оның 5 'ұшын РНҚ праймері мен ДНҚ-ның кішкене сегментін ығыстырады. Бұл РНҚ-ДНҚ бір тізбекті қақпағын тудырады, оны бөліп алу керек, және екі Оказаки фрагменттері арасындағы никті ДНК-лигаза I тығыздау керек. Бұл процесс Оказаки фрагментінің жетілуі деп аталады және оны екі жолмен өңдеуге болады: бір механизм процестері қысқа қақпақтар, ал басқалары ұзын қақпақтармен айналысады.[85] ДНҚ-полимераза δ өзінің полимерленуінен бұрын ДНҚ немесе РНҚ-ның 2-ден 3-ке дейін нуклеотидтерін ығыстыра алады, бұл үшін қысқа «қақпақты» субстрат түзеді. Фен1, ол нуклеотидтерді жапқыштан алып тастай алады, бір уақытта бір нуклеотид.
Осы процестің циклдарын қайталай отырып, ДНҚ-полимераза δ және Fen1 РНҚ праймерлерін кетіруді үйлестіре алады және артта қалған ДНҚ никін қалдыра алады.[86] Бұл қайталанатын процесс жасушадан гөрі ұтымды реттелгендіктен және оны шығарып тастау керек үлкен қақпақтар жасамайтындықтан жақсырақ деген ұсыныс жасалды.[87] Фен1 / ДНҚ-полимераза δ белсенділігі реттелмеген жағдайда, жасуша Dna2 қолдану арқылы ұзын қақпақтарды генерациялау және өңдеу үшін альтернативті механизмді пайдаланады, оның құрамында геликаза және нуклеаза белсенділігі бар.[88] Dna2-нің нуклеазалық белсенділігі осы ұзын қақпақтарды алып тастау үшін қажет, ал Fen1 өңдейтін қысқа қақпақ қалдырады. Электронды микроскопия Зерттеулер көрсеткендей, артта қалған жіпке нуклеосоманың жүктелуі синтез орнына өте жақын болады.[89] Осылайша, Оказаки фрагментінің жетілуі - бұл пайда болатын ДНҚ синтезделгеннен кейін пайда болатын тиімді процесс.
Репликативті ДНҚ-полимеразалар
Репликативті геликаза ата-аналық ДНҚ дуплексін ашқаннан кейін, екі бір тізбекті ДНҚ шаблондарын шығарғаннан кейін, ата-аналық геномның екі данасын жасау үшін репликативті полимеразалар қажет. ДНҚ-полимеразаның қызметі жоғары мамандандырылған және нақты шаблондарда және тар локализацияларда репликацияны орындайды. Эукариоттық репликация шанышқысында ДНҚ репликациясына ықпал ететін үш репликативті полимеразалық кешендер бар: Полимераза α, Полимераза δ және Полимераза ε. Бұл үш полимераза жасушаның өміршеңдігі үшін өте маңызды.[90]
ДНҚ полимеразаларына ДНҚ синтезін бастауға арналған праймер қажет болғандықтан, полимераза α (Pol α) репликативті примаза ретінде әрекет етеді. Pol α РНҚ-примазамен байланысты және бұл кешен РНҚ-ның қысқа 10 нуклеотидтік созылуын, содан кейін 10-нан 20-ға дейін ДНҚ негіздерін қамтитын праймерді синтездеу арқылы алғашқы тапсырманы орындайды.[3] Маңыздысы, бұл алғашқы әрекет синтезді бастау үшін репликация басталған кезде пайда болады, сонымен қатар артта қалған жіптегі әрбір Оказаки фрагментінің 5 'соңында пайда болады.
Алайда Pol α ДНҚ репликациясын жалғастыра алмайды және оны ДНҚ синтезін жалғастыру үшін басқа полимеразамен алмастыру керек.[91] Полимеразды ауыстырып қосу үшін қысқыш тиегіштер қажет және ДНҚ-ны қалыпты репликациялау үшін барлық үш ДНҚ полимеразаларының үйлестірілген әрекеттері қажет екендігі дәлелденді: синтезді бастау үшін Pol α, жетекші репликация үшін Pol ε және генерациялау үшін үнемі жүктелетін Pol δ. Синдромның артта қалуы кезіндегі Оказаки фрагменттері.[92]
- Полимераза α (Пол α): Шағын каталитикалық суббірлікпен (PriS) және үлкен каталитикалық емес (PriL) суббірлікпен комплекс түзеді.[93] Біріншіден, РНҚ праймерінің синтезі ДНҚ-полимераз альфа арқылы ДНҚ синтезделуіне мүмкіндік береді. Бір рет жетекші тізбекте және әр артта қалған Оказаки фрагментінің басында пайда болады. При суббірліктері РНҚ праймерін синтездей отырып, примаза рөлін атқарады. ДНҚ Пол α жаңадан пайда болған праймерді ДНҚ нуклеотидтерімен ұзартады. 20-ға жуық нуклеотидтерден кейін созылуды жетекші тізбекте Pol and, ал артта қалуда Pol δ қабылдайды.[94]
- Полимераза δ (Пол δ): Жоғары технологиялық және корректорлық, 3 '-> 5' экзонуклеазалық белсенділігі бар. In vivo, ол екі полимеразаның артта қалуына да қатысады және жетекші синтез.[95]
- Полимераза ε (Пол ε): Жоғары технологиялық және корректорлық, 3 '-> 5' экзонуклеазалық белсенділігі бар. Pol to-мен өте байланысты, in vivo ол негізінен pol δ қателерін тексеруде жұмыс істейді.[95]
Cdc45 – Mcm – GINS helicase кешені
ДНҚ геликаздар және полимеразалар репликация шанышқысында тығыз байланыста болуы керек. Егер шешілу синтезден әлдеқайда бұрын пайда болса, онда бір тізбекті ДНҚ-ның үлкен жолдары ұшырасады. Бұл ДНҚ зақымдану сигналын белсендіруі немесе ДНҚ-ны қалпына келтіру процестерін тудыруы мүмкін. Бұл проблемаларды болдырмау үшін эукариоттық реписисомада репликация шанышқысының алдында геликазаның белсенділігін реттеуге арналған мамандандырылған ақуыздар бар. Бұл ақуыздар геликазалар мен полимеразалар арасындағы физикалық өзара әрекеттесу үшін түйісетін жерлерді қамтамасыз етеді, осылайша дуплексті босатуды ДНҚ синтезімен байланыстырады.[96]
ДНҚ-полимеразалардың жұмыс істеуі үшін екі тізбекті ДНҚ спиралын репликациялау үшін екі бір тізбекті ДНҚ шаблондарын ашуға болмайды. ДНҚ-геликазалар хромосомалардың репликациясы кезінде екі тізбекті ДНҚ-ны шешуге жауапты. Эукариотты жасушалардағы геликазалар өте күрделі.[97] Геликазаның каталитикалық ядросы алты минихромосоманың күтімі (Mcm2-7) құрайды, гексамерикалық сақина. ДНҚ-дан алыс Mcm2-7 ақуыздары біртұтас гетерогексамер түзеді және ДНҚ-ның репликациясының бастауларында белсенді емес түрде екі тізбекті ДНҚ айналасында бас-бас қос гексамерлер ретінде жүктеледі.[97][98] Mcm ақуыздары репликация бастауларына қабылданады, содан кейін S фазасында бүкіл геномдық ДНҚ-да қайта бөлінеді, бұл олардың репликация шанышқысына локализациясын көрсетеді.[47]
Mcm ақуыздарының жүктелуі тек G кезінде болуы мүмкін1 of the cell cycle, and the loaded complex is then activated during S phase by recruitment of the Cdc45 protein and the GINS complex to form the active Cdc45–Mcm–GINS (CMG) helicase at DNA replication forks.[99][100] Mcm activity is required throughout the S phase for DNA replication.[35][101] A variety of regulatory factors assemble around the CMG helicase to produce the ‘Replisome Progression Complex’ which associates with DNA polymerases to form the eukaryotic replisome, the structure of which is still quite poorly defined in comparison with its bacterial counterpart.[53][102]
The isolated CMG helicase and Replisome Progression Complex contain a single Mcm protein ring complex suggesting that the loaded double hexamer of the Mcm proteins at origins might be broken into two single hexameric rings as part of the initiation process, with each Mcm protein complex ring forming the core of a CMG helicase at the two replication forks established from each origin.[53][99] The full CMG complex is required for DNA unwinding, and the complex of CDC45-Mcm-GINS is the functional DNA helicase in eukaryotic cells.[103]
Ctf4 and And1 proteins
The CMG complex interacts with the replisome through the interaction with Ctf4 and And1 proteins. Ctf4/And1 proteins interact with both the CMG complex and DNA polymerase α.[104] Ctf4 is a polymerase α accessory factor, which is required for the recruitment of polymerase α to replication origins.[105]
Mrc1 and Claspin proteins
Mrc1/Claspin proteins couple leading-strand synthesis with the CMG complex helicase activity. Mrc1 interacts with polymerase ε as well as Mcm proteins.[106] The importance of this direct link between the helicase and the leading-strand polymerase is underscored by results in cultured human cells, where Mrc1/Claspin is required for efficient replication fork progression.[107] These results suggest that efficient DNA replication also requires the coupling of helicases and leading-strand synthesis...
Пролиферацияланатын жасушалық ядролық антиген
DNA polymerases require additional factors to support DNA replication. DNA polymerases have a semiclosed 'hand' structure, which allows the polymerase to load onto the DNA and begin translocating. This structure permits DNA polymerase to hold the single-stranded DNA template, incorporate dNTPs at the active site, and release the newly formed double-stranded DNA. However, the structure of DNA polymerases does not allow a continuous stable interaction with the template DNA.[1]
To strengthen the interaction between the polymerase and the template DNA, DNA sliding clamps associate with the polymerase to promote the processivity of the replicative polymerase. In eukaryotes, the sliding clamp is a homotrimer ring structure known as the proliferating cell nuclear antigen (PCNA). The PCNA ring has polarity with surfaces that interact with DNA polymerases and tethers them securely to the DNA template. PCNA-dependent stabilization of DNA polymerases has a significant effect on DNA replication because PCNAs are able to enhance the polymerase processivity up to 1,000-fold.[108][109] PCNA is an essential cofactor and has the distinction of being one of the most common interaction platforms in the replisome to accommodate multiple processes at the replication fork, and so PCNA is also viewed as a regulatory cofactor for DNA polymerases.[110]
Репликация коэффициенті C
PCNA fully encircles the DNA template strand and must be loaded onto DNA at the replication fork. At the leading strand, loading of the PCNA is an infrequent process, because DNA replication on the leading strand is continuous until replication is terminated. However, at the lagging strand, DNA polymerase δ needs to be continually loaded at the start of each Okazaki fragment. This constant initiation of Okazaki fragment synthesis requires repeated PCNA loading for efficient DNA replication.
PCNA loading is accomplished by the репликация коэффициенті C (RFC) complex. The RFC complex is composed of five ATPases: Rfc1, Rfc2, Rfc3, Rfc4 and Rfc5.[111] RFC recognizes primer-template junctions and loads PCNA at these sites.[112][113] The PCNA homotrimer is opened by RFC by ATP hydrolysis and is then loaded onto DNA in the proper orientation to facilitate its association with the polymerase.[114][115] Clamp loaders can also unload PCNA from DNA; a mechanism needed when replication must be terminated.[115]
Stalled replication fork
ДНҚ репликациясы at the replication fork can be halted by a shortage of deoxynucleotide triphosphates (dNTPs) or by DNA damage, resulting in репликациялық стресс.[116] This halting of replication is described as a stalled replication fork. A fork protection complex of proteins stabilizes the replication fork until DNA damage or other replication problems can be fixed.[116] Prolonged replication fork stalling can lead to further DNA damage. Stalling signals are deactivated if the problems causing the replication fork are resolved.[116]
Тоқтату

Termination of eukaryotic DNA replication requires different processes depending on whether the chromosomes are circular or linear. Unlike linear molecules, circular chromosomes are able to replicate the entire molecule. However, the two DNA molecules will remain linked together. This issue is handled by decatenation of the two DNA molecules by a type II topoisomerase. Type II topoisomerases are also used to separate linear strands as they are intricately folded into a nucleosome within the cell.
As previously mentioned, linear chromosomes face another issue that is not seen in circular DNA replication. Due to the fact that an RNA primer is required for initiation of DNA synthesis, the lagging strand is at a disadvantage in replicating the entire chromosome. While the leading strand can use a single RNA primer to extend the 5' terminus of the replicating DNA strand, multiple RNA primers are responsible for lagging strand synthesis, creating Okazaki fragments. This leads to an issue due to the fact that DNA polymerase is only able to add to the 3' end of the DNA strand. The 3'-5' action of DNA polymerase along the parent strand leaves a short single-stranded DNA (ssDNA) region at the 3' end of the parent strand when the Okazaki fragments have been repaired. Since replication occurs in opposite directions at opposite ends of parent chromosomes, each strand is a lagging strand at one end. Over time this would result in progressive shortening of both daughter chromosomes. This is known as the end replication problem.[1]
The end replication problem is handled in eukaryotic cells by telomere аймақтар және теломераза. Telomeres extend the 3' end of the parental chromosome beyond the 5' end of the daughter strand. This single-stranded DNA structure can act as an origin of replication that recruits telomerase. Telomerase is a specialized DNA polymerase that consists of multiple protein subunits and an RNA component. The RNA component of telomerase anneals to the single stranded 3' end of the template DNA and contains 1.5 copies of the telomeric sequence.[84] Telomerase contains a protein subunit that is a кері транскриптаза деп аталады telomerase reverse transcriptase or TERT. TERT synthesizes DNA until the end of the template telomerase RNA and then disengages.[84] This process can be repeated as many times as needed with the extension of the 3' end of the parental DNA molecule. This 3' addition provides a template for extension of the 5' end of the daughter strand by lagging strand DNA synthesis. Regulation of telomerase activity is handled by telomere-binding proteins.
Replication fork barriers
Prokaryotic DNA replication is bidirectional; within a replicative origin, replisome complexes are created at each end of the replication origin and replisomes move away from each other from the initial starting point. In prokaryotes, bidirectional replication initiates at one replicative origin on the circular chromosome and terminates at a site opposed from the initial start of the origin.[117] These termination regions have DNA sequences known as Тер сайттар. Мыналар Тер sites are bound by the Tus protein. The Тер-Tus complex is able to stop helicase activity, terminating replication.[118]
In eukaryotic cells, termination of replication usually occurs through the collision of the two replicative forks between two active replication origins. The location of the collision varies on the timing of origin firing. In this way, if a replication fork becomes stalled or collapses at a certain site, replication of the site can be rescued when a replisome traveling in the opposite direction completes copying the region. There are programmed replication fork barriers (RFBs) bound by RFB proteins in various locations, throughout the genome, which are able to terminate or pause replication forks, stopping progression of the replisome.[117]
Replication factories
It has been found that replication happens in a localised way in the cell nucleus. Contrary to the traditional view of moving replication forks along stagnant DNA, a concept of replication factories emerged, which means replication forks are concentrated towards some immobilised 'factory' regions through which the template DNA strands pass like conveyor belts. [119]
Жасуша циклін реттеу
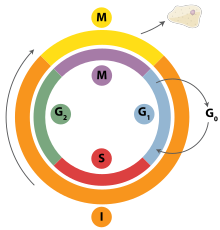
DNA replication is a tightly orchestrated process that is controlled within the context of the жасушалық цикл. Progress through the cell cycle and in turn DNA replication is tightly regulated by the formation and activation of pre-replicative complexes (pre-RCs) which is achieved through the activation and inactivation of циклинге тәуелді киназалар (Cdks, CDKs). Specifically it is the interactions of циклиндер and cyclin dependent kinases that are responsible for the transition from G1 into S-phase.
During the G1 phase of the cell cycle there are low levels of CDK activity. This low level of CDK activity allows for the formation of new pre-RC complexes but is not sufficient for DNA replication to be initiated by the newly formed pre-RCs. During the remaining phases of the cell cycle there are elevated levels of CDK activity. This high level of CDK activity is responsible for initiating DNA replication as well as inhibiting new pre-RC complex formation.[2] Once DNA replication has been initiated the pre-RC complex is broken down. Due to the fact that CDK levels remain high during the S phase, G2, and M phases of the cell cycle no new pre-RC complexes can be formed. This all helps to ensure that no initiation can occur until the cell division is complete.
In addition to cyclin dependent kinases a new round of replication is thought to be prevented through the downregulation of Cdt1. This is achieved via degradation of Cdt1 as well as through the inhibitory actions of a protein known as геминин. Geminin binds tightly to Cdt1 and is thought to be the major inhibitor of re-replication.[2] Geminin first appears in S-phase and is degraded at the metaphase-anaphase transition, possibly through ubiquination by анафазаны жылжытатын кешен (APC).[120]
Әр түрлі ұялы циклды бақылау нүктелері are present throughout the course of the cell cycle that determine whether a cell will progress through division entirely. Importantly in replication the G1, or restriction, checkpoint makes the determination of whether or not initiation of replication will begin or whether the cell will be placed in a resting stage known as G0. Cells in the G0 stage of the cell cycle are prevented from initiating a round of replication because the minichromosome maintenance proteins are not expressed. Transition into the S-phase indicates replication has begun.
Replication checkpoint proteins
In order to preserve genetic information during cell division, DNA replication must be completed with high fidelity. In order to achieve this task, eukaryotic cells have proteins in place during certain points in the replication process that are able to detect any errors during DNA replication and are able to preserve genomic integrity. These checkpoint proteins are able to stop the cell cycle from entering mitosis in order to allow time for DNA repair. Checkpoint proteins are also involved in some DNA repair pathways, while they stabilize the structure of the replication fork to prevent further damage. These checkpoint proteins are essential to avoid passing down mutations or other chromosomal aberrations to offspring.
Eukaryotic checkpoint proteins are well conserved and involve two phosphatidylinositol 3-kinase-related kinases (PIKKs), ATR және Банкомат. Both ATR and ATM share a target phosphorylation sequence, the SQ/TQ motif, but their individual roles in cells differ.[121]
ATR is involved in arresting the cell cycle in response to DNA double-stranded breaks. ATR has an obligate checkpoint partner, ATR-interacting-protein (ATRIP), and together these two proteins are responsive to stretches of single-stranded DNA that are coated by replication protein A (RPA).[122] The formation of single-stranded DNA occurs frequently, more often during replication stress. ATR-ATRIP is able to arrest the cell cycle to preserve genome integrity. ATR is found on chromatin during S phase, similar to RPA and claspin.[123]
The generation of single-stranded DNA tracts is important in initiating the checkpoint pathways downstream of replication damage. Once single-stranded DNA becomes sufficiently long, single-stranded DNA coated with RPA are able to recruit ATR-ATRIP.[124] In order to become fully active, the ATR kinase rely on sensor proteins that sense whether the checkpoint proteins are localized to a valid site of DNA replication stress. The RAD9 -HUS1 -Rad1 (9-1-1) heterotrimeric clamp and its clamp loader RFCRad17 are able to recognize gapped or nicked DNA. The RFCRad17 clamp loader loads 9-1-1 onto the damaged DNA.[125] The presence of 9-1-1 on DNA is enough to facilitate the interaction between ATR-ATRIP and a group of proteins termed checkpoint mediators, such as TOPBP1 and Mrc1/claspin. TOPBP1 interacts with and recruits the phosphorylated Rad9 component of 9-1-1 and binds ATR-ATRIP, which phosphorylates Chk1.[126] Mrc1/Claspin is also required forthe complete activation of ATR-ATRIP that phosphorylates Chk1, the major downstream checkpoint effector kinase.[127] Claspin is a component of the replisome and contains a domain for docking with Chk1, revealing a specific function of Claspin during DNA replication: the promotion ofcheckpoint signaling at the replisome.[128]
Chk1 signaling is vital for arresting the cell cycle and preventing cells from entering mitosis with incomplete DNA replication or DNA damage. The Chk1-dependent Cdk inhibition is important for the function of the ATR-Chk1 checkpoint and to arrest the cell cycle and allow sufficient time for completion of DNA repair mechanisms, which in turn prevents the inheritance of damaged DNA. In addition, Chk1-dependent Cdk inhibition plays a critical role in inhibiting origin firing during S phase. This mechanism prevents continued DNA synthesis and is required for the protection of the genome in thepresence of replication stress and potential genotoxic conditions.[129] Thus, ATR-Chk1 activity further prevents potential replication problems at the level of single replication origins by inhibiting initiation of replication throughout the genome, until the signaling cascade maintaining cell-cycle arrest is turned off.
Replication through nucleosomes

Eukaryotic DNA must be tightly compacted in order to fit within the confined space of the nucleus. Chromosomes are packaged by wrapping 147 nucleotides around an octamer of гистон proteins, forming a нуклеосома. The nucleosome octamer includes two copies of each histone H2A, H2B, H3, және H4. Due to the tight association of histone proteins to DNA, eukaryotic cells have proteins that are designed to remodel histones ahead of the replication fork, in order to allow smooth progression of the replisome.[130] There are also proteins involved in reassembling histones behind the replication fork to reestablish the nucleosome conformation.[131]
There are several histone chaperones that are known to be involved in nucleosome assembly after replication. The ШЫНДЫҚ complex has been found to interact with DNA polymerase α-primase complex, and the subunits of the FACT complex interacted genetically with replication factors.[132][133] The FACT complex is a heterodimer that does not hydrolyze ATP, but is able to facilitate "loosening" of histones in nucleosomes, but how the FACT complex is able to relieve the tight association of histones for DNA removal remains unanswered.[134]
Another histone chaperone that associates with the replisome is Asf1, which interacts with the Mcm complex dependent on histone dimers H3-H4.[135] Asf1 is able to pass newly synthesized H3-H4 dimer to deposition factors behind the replication fork and this activity makes the H3-H4 histone dimers available at the site of histone deposition just after replication.[136] Asf1 (and its partner Rtt109) has also been implicated in inhibiting gene expression from replicated genes during S-phase.[137]
The heterotrimeric chaperone chromatin assembly factor 1 (CAF-1 ) is a chromatin formation protein that is involved in depositing histones onto both newly replicated DNA strands to form chromatin.[138] CAF-1 contains a PCNA-binding motif, called a PIP-box, that allows CAF-1 to associate with the replisome through PCNA and is able to deposit histone H3-H4 dimers onto newly synthesized DNA.[139][140] The Rtt106 chaperone is also involved in this process, and associated with CAF-1 and H3-H4 dimers during chromatin formation.[141] These processes load newly synthesized histones onto DNA.
After the deposition of histones H3-H4, nucleosomes form by the association of histone H2A-H2B. This process is thought to occur through the FACT complex, since it already associated with the replisome and is able to bind free H2A-H2B, or there is the possibility of another H2A-H2B chaperone, Nap1.[142] Electron microscopy studies show that this occurs very quickly, as nucleosomes can be observed forming just a few hundred base pairs after the replication fork.[143] Therefore, the entire process of forming newnucleosomes takes place just after replication due to the coupling of histone chaperones to the replisome.
Comparisons between prokaryotic and eukaryotic DNA replication
When compared to prokaryotic DNA replication, the completion of eukaryotic DNA replication is more complex and involves multiple origins of replication and replicative proteins to accomplish. Prokaryotic DNA is arranged in a circular shape, and has only one replication origin when replication starts. By contrast, eukaryotic DNA is linear. When replicated, there are as many as one thousand origins of replication.[144]
Eukaryotic DNA is bidirectional. Here the meaning of the word bidirectional is different. Eukaryotic linear DNA has many origins (called O) and termini (called T). "T" is present to the right of "O". One "O" and one "T" together form one replicon. After the formation of pre-initiation complex, when one replicon starts elongation, initiation starts in second replicon. Now, if the first replicon moves in clockwise direction, the second replicon moves in anticlockwise direction, until "T" of first replicon is reached. At "T", both the replicons merge to complete the process of replication. Meanwhile, the second replicon is moving in forward direction also, to meet with the third replicon. This clockwise and counter-clockwise movement of two replicons is termed as bidirectional replication.
Eukaryotic DNA replication requires precise coordination of all DNA polymerases and associated proteins to replicate the entire genome each time a cell divides. This process is achieved through a series of steps of protein assemblies at origins of replication, mainly focusing the regulation of DNA replication on the association of the MCM helicase with the DNA. These origins of replication direct the number of protein complexes that will form to initiate replication. In prokaryotic DNA replication regulation focuses on the binding of the DnaA initiator protein to the DNA, with initiation of replication occurring multiple times during one cell cycle.[84] Both prokaryotic and eukaryotic DNA use ATP binding and hydrolysis to direct helicase loading and in both cases the helicase is loaded in the inactive form. However, eukaryotic helicases are double hexamers that are loaded onto double stranded DNA whereas prokaryotic helicases are single hexamers loaded onto single stranded DNA.[145]
Segregation of chromosomes is another difference between prokaryotic and eukaryotic cells. Rapidly dividing cells, such as bacteria, will often begin to segregate chromosomes that are still in the process of replication. In eukaryotic cells chromosome segregation into the daughter cells is not initiated until replication is complete in all chromosomes.[84] Despite these differences, however, the underlying process of replication is similar for both prokaryotic and eukaryotic DNA.
| Prokaryotic DNA Replication | Эукариотты ДНҚ репликациясы |
|---|---|
| Occurs inside the cytoplasm | Occurs inside the nucleus |
| Only one origin of replication per molecule of DNA | Have many origins of replication in each chromosome |
| Origin of replication is about 100-200 or more nucleotides in length | Each origin of replication is formed of about 150 nucleotides |
| Replication occurs at one point in each chromosome | Replication occurs at several points simultaneously in each chromosome |
| Only have one origin of replication | Has multiple origins of replication |
| Initiation is carried out by protein DnaA and DnaB | Initiation is carried out by the Origin Recognition Complex |
| Topoisomerase is needed | Topoisomerase is needed |
| Replication is very rapid | Replication is very slow |
Eukaryotic DNA replication protein list
List of major proteins involved in eukaryotic DNA replication:
| Ақуыз | Function in Eukaryotic DNA replication |
|---|---|
| ЖӘНЕ1 | Loads DNA polymerase α onto chromatin together with CMG complex on the lagging strand. Also known as Ctf4 in budding yeast. |
| Cdc45 | Required for initiation and elongation steps of DNA replication. A part of the Mcm2-7 helicase complex. Required after pre-RC step for loading of various proteins for initiation and elongation. |
| Cdc45-Mcm-GINS (CMG) complex | Functional DNA helicase in eukaryotic cells |
| CD6 | Required for assembly of Mcm2-7 complex at ORC, in conjunction with Cdt1 . |
| Cdc7-Dbf4 kinase or Dbf4-dependent kinase (DDK) | Protein kinase required for initiation of DNA replication, probably through phosphorylation of the minichromosome maintenance proteins. |
| Cdt1 | Loads Mcm2-7 complex on DNA at ORC in pre-RC/licensing step. Inhibited in metazoans by geminin. |
| Класпин | Couple leading-strand synthesis with the CMG complex helicase activity. Works with Mrc1 |
| Ctf4 | Loads DNA polymerase α onto chromatin together with CMG complex on the lagging strand. Homolog in metazoans is known as AND-1. |
| Циклинге тәуелді киназа (CDK) | Cyclin-dependent protein kinase required for initiation of replication and for other subsequent steps. |
| Dna2 | 5' flap endonuclease and helicase involved in processing Okazaki fragments. |
| ДНҚ лигазы I | Joins Okazaki fragments during DNA replication. Ligase activity also needed for DNA repair and recombination. |
| DNA polymerase α (Pol α) | Contains primase activity that is necessary to initiate DNA synthesis on both leading and lagging strands. |
| ДНҚ-полимераза δ (Pol δ) | Required to complete synthesis of Okazaki fragments on the lagging strand that have been started by DNA polymerase α. |
| DNA polymerase ε (Pol ε) | The leading strand polymerase. Synthesizes DNA at the replication fork. Binds early at origins via Dbp11 and needed to load DNA polymerase α. |
| Dpb11 | DNA replication initiation protein. Loads DNA polymerase ε onto pre-replication complexes at origins. |
| Fen1 | 5' flap endonuclease involved in processing Okazaki fragments. |
| Геминин | Protein found in metazoans and absent from yeasts. Binds to and inactivates Cdt1, thereby regulating pre-replicative/initiation complex formation. Also suggested to promote pre-RC formation by binding and thus preventing Cdt1 degradation |
| GINS | Tetrameric complex composed of Sld5, Psf1, Psf2, Psf3. Associates with pre-replicative complex around the time of initiation and moves with replication forks during elongation step. Required for elongation stage of DNA replication and maybe part of the Mcm helicase complex. |
| Minichromosome maintenance proteins (Mcm) | Six different proteins of the AAA+ ATPase family that form a hexamer in solution. This hexamer is recruited and loaded by ORC, Cdc6 and Cdt1 and forms a double hexamer that is topologically linked around DNA to form a salt-resistant pre-replicative complex. On replication initiation, Mcm2-7 moves away from ORC with replication fork. |
| Mcm10 | Required for initiation and elongation stages of DNA replication. Implicated in chromatin binding of Cdc45 and DNA polymerase α. Also required for stability of DNA polymerase α catalytic subunit in the budding yeast S. cerevisiae. |
| Mrc1 | Couple leading-strand synthesis with the CMG complex helicase activity. Metazoan homolog is known as Claspin. |
| Шығу тегін тану кешені (ORC) | Heterohexameric complex composed of Orc1–Orc6 proteins. Binds to DNA and assembles Mcm2-7 complex onto chromatin together with Cdc6 and Cdt1. |
| Пролиферацияланатын жасушалық ядролық антиген (PCNA) | Trimeric protein with ring shaped structure, encloses DNA preventing dissociation of DNA polymerase. Acts as a sliding clamp for polymerases δ and ε, thereby improving processivity of replicative polymerases. |
| Репликация коэффициенті C (RFC) | Loads PCNA on primed templates and is involved in the switch between DNA polymerase a and the replicative polymerases δ and ε. |
| Replication fork barriers (RFBs) | Bound by RFB proteins in various locations throughout the genome. Are able to terminate or pause replication forks, stopping progression of the replisome. |
| Ақуыздың репликациясы (RPA) | Heterotrimeric single-stranded binding protein. Stabilizes single-stranded DNA at replication fork. |
| RNase H | Ribonuclease which digests RNA hybridized to DNA. Involved in Okazaki fragment processing. |
| Sld2 | Functions in initiation of replication. Key substrate of CDK, phosphorylation promotes interaction with Dpb11. Required for initiation of replication. |
| Sld3 | Functions in initiation of replication. Key substrate of CDK, phosphorylation promotes interaction with Dpb11. Required for initiation of replication. |
| Теломераза | A ribonucleoprotein that adds DNA sequence "TTAGGG" repeats to the 3' end of DNA strands in telomeres. |
| Topoisomerases | Regulate the overwinding or underwinding of DNA |
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ а б c г. Leman AR, Noguchi E (March 2013). "The replication fork: understanding the eukaryotic replication machinery and the challenges to genome duplication". Гендер. 4 (1): 1–32. дои:10.3390/genes4010001. PMC 3627427. PMID 23599899.
- ^ а б c г. Blow JJ, Dutta A (June 2005). "Preventing re-replication of chromosomal DNA". Молекулалық жасуша биологиясының табиғаты туралы шолулар. 6 (6): 476–86. дои:10.1038/nrm1663. PMC 2688777. PMID 15928711.
- ^ а б Fisher PA, Wang TS, Korn D (July 1979). "Enzymological characterization of DNA polymerase alpha. Basic catalytic properties processivity, and gap utilization of the homogeneous enzyme from human KB cells". Биологиялық химия журналы. 254 (13): 6128–37. PMID 447699.
- ^ Araki H (2011). "Initiation of chromosomal DNA replication in eukaryotic cells; contribution of yeast genetics to the elucidation". Гендер және генетикалық жүйелер. 86 (3): 141–9. дои:10.1266/ggs.86.141. PMID 21952204.
- ^ Майорано Д, Моро Дж, Мехали М (сәуір 2000). «XCDT1 Xenopus laevis-те репликативті кешендерді құрастыру үшін қажет». Табиғат. 404 (6778): 622–5. Бибкод:2000 ж. Табиғат. 404..622М. дои:10.1038/35007104. PMID 10766247. S2CID 4416138.
- ^ а б c Bell SP, Dutta A (2002). "DNA replication in eukaryotic cells". Биохимияның жылдық шолуы. 71: 333–74. дои:10.1146/annurev.biochem.71.110601.135425. PMID 12045100.
- ^ Tye BK (1999). "MCM proteins in DNA replication". Биохимияның жылдық шолуы. 68 (1): 649–86. дои:10.1146/annurev.biochem.68.1.649. PMID 10872463.
- ^ Ticau S, Friedman LJ, Ivica NA, Gelles J, Bell SP (April 2015). "Single-molecule studies of origin licensing reveal mechanisms ensuring bidirectional helicase loading". Ұяшық. 161 (3): 513–525. дои:10.1016/j.cell.2015.03.012. PMC 4445235. PMID 25892223.
- ^ а б Zhai Y, Li N, Jiang H, Huang X, Gao N, Tye BK (July 2017). "Unique Roles of the Non-identical MCM Subunits in DNA Replication Licensing". Молекулалық жасуша. 67 (2): 168–179. дои:10.1016/j.molcel.2017.06.016. PMID 28732205.
- ^ Coster G, Diffley JF (July 2017). "Bidirectional eukaryotic DNA replication is established by quasi-symmetrical helicase loading". Ғылым. 357 (6348): 314–318. Бибкод:2017Sci...357..314C. дои:10.1126/science.aan0063. PMC 5608077. PMID 28729513.
- ^ а б c г. e Zhai Y, Cheng E, Wu H, Li N, Yung PY, Gao N, Tye BK (March 2017). "Open-ringed structure of the Cdt1-Mcm2-7 complex as a precursor of the MCM double hexamer". Табиғат құрылымы және молекулалық биология. 24 (3): 300–308. дои:10.1038/nsmb.3374. PMID 28191894. S2CID 3929807.
- ^ Bell SP (March 2002). "The origin recognition complex: from simple origins to complex functions". Гендер және даму. 16 (6): 659–72. дои:10.1101/gad.969602. PMID 11914271.
- ^ Bell, S. P.; Stillman, B. (1992-05-14). "ATP-dependent recognition of eukaryotic origins of DNA replication by a multiprotein complex". Табиғат. 357 (6374): 128–134. Бибкод:1992 ж.357..128B. дои:10.1038 / 357128a0. ISSN 0028-0836. PMID 1579162. S2CID 4346767.
- ^ а б c г. e f Li N, Lam WH, Zhai Y, Cheng J, Cheng E, Zhao Y, Gao N, Tye BK (July 2018). "Structure of the origin recognition complex bound to DNA replication origin". Табиғат. 559 (7713): 217–222. Бибкод:2018Natur.559..217L. дои:10.1038/s41586-018-0293-x. PMID 29973722. S2CID 49577101.
- ^ Miotto B, Ji Z, Struhl K (August 2016). "Selectivity of ORC binding sites and the relation to replication timing, fragile sites, and deletions in cancers". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 113 (33): E4810-9. дои:10.1073/pnas.1609060113. PMC 4995967. PMID 27436900.
- ^ Bleichert F, Leitner A, Aebersold R, Botchan MR, Berger JM (June 2018). "Conformational control and DNA-binding mechanism of the metazoan origin recognition complex". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 115 (26): E5906–E5915. дои:10.1073/pnas.1806315115. PMC 6042147. PMID 29899147.
- ^ Chesnokov IN (2007). "Multiple functions of the origin recognition complex". Халықаралық цитология шолу. 256: 69–109. дои:10.1016/S0074-7696(07)56003-1. ISBN 9780123737007. PMID 17241905.
- ^ Matsuda K, Makise M, Sueyasu Y, Takehara M, Asano T, Mizushima T (December 2007). "Yeast two-hybrid analysis of the origin recognition complex of Saccharomyces cerevisiae: interaction between subunits and identification of binding proteins". FEMS ашытқыларын зерттеу. 7 (8): 1263–9. дои:10.1111/j.1567-1364.2007.00298.x. PMID 17825065.
- ^ Kreitz S, Ritzi M, Baack M, Knippers R (March 2001). "The human origin recognition complex protein 1 dissociates from chromatin during S phase in HeLa cells". Биологиялық химия журналы. 276 (9): 6337–42. дои:10.1074/jbc.M009473200. PMID 11102449.
- ^ Speck C, Chen Z, Li H, Stillman B (November 2005). "ATPase-dependent cooperative binding of ORC and Cdc6 to origin DNA". Табиғат құрылымы және молекулалық биология. 12 (11): 965–71. дои:10.1038/nsmb1002. PMC 2952294. PMID 16228006.
- ^ Coleman TR, Carpenter PB, Dunphy WG (October 1996). "The Xenopus Cdc6 protein is essential for the initiation of a single round of DNA replication in cell-free extracts". Ұяшық. 87 (1): 53–63. дои:10.1016/S0092-8674(00)81322-7. PMID 8858148. S2CID 16897247.
- ^ Rialland M, Sola F, Santocanale C (April 2002). «ДНҚ репликациясындағы және хроматинді лицензиялаудағы адамның CDT1 маңызды рөлі». Cell Science журналы. 115 (Pt 7): 1435-40. PMID 11896191.
- ^ Tanaka S, Diffley JF (March 2002). "Interdependent nuclear accumulation of budding yeast Cdt1 and Mcm2-7 during G1 phase". Табиғи жасуша биологиясы. 4 (3): 198–207. дои:10.1038/ncb757. PMID 11836525. S2CID 45861829.
- ^ Frigola J, He J, Kinkelin K, Pye VE, Renault L, Douglas ME, Remus D, Cherepanov P, Costa A, Diffley JF (June 2017). "Cdt1 stabilizes an open MCM ring for helicase loading". Табиғат байланысы. 8: 15720. Бибкод:2017NatCo...815720F. дои:10.1038/ncomms15720. PMC 5490006. PMID 28643783.
- ^ Ticau S, Friedman LJ, Champasa K, Corrêa IR, Gelles J, Bell SP (March 2017). "Mechanism and timing of Mcm2-7 ring closure during DNA replication origin licensing". Табиғат құрылымы және молекулалық биология. 24 (3): 309–315. дои:10.1038/nsmb.3375. PMC 5336523. PMID 28191892.
- ^ Nishitani H, Lygerou Z, Nishimoto T, Nurse P (April 2000). «Cdt1 ақуызы бөлінетін ашытқыдағы репликация үшін ДНҚ-ны лицензиялау үшін қажет». Табиғат. 404 (6778): 625–8. Бибкод:2000 ж. Табиғат. 404..625N. дои:10.1038/35007110. PMID 10766248. S2CID 205005540.
- ^ Yuan Z, Riera A, Bai L, Sun J, Nandi S, Spanos C, Chen ZA, Barbon M, Rappsilber J, Stillman B, Speck C, Li H (March 2017). "Structural basis of Mcm2-7 replicative helicase loading by ORC-Cdc6 and Cdt1". Табиғат құрылымы және молекулалық биология. 24 (3): 316–324. дои:10.1038/nsmb.3372. PMC 5503505. PMID 28191893.
- ^ Wohlschlegel JA, Dwyer BT, Dhar SK, Cvetic C, Walter JC, Dutta A (желтоқсан 2000). «Гемининнің Cdt1 байланыстыруымен эукариотты ДНҚ репликациясының тежелуі». Ғылым. 290 (5500): 2309–12. Бибкод:2000Sci ... 290.2309W. дои:10.1126 / ғылым.290.5500.2309. PMID 11125146.
- ^ Maine GT, Sinha P, Tye BK (March 1984). "Mutants of S. cerevisiae defective in the maintenance of minichromosomes". Генетика. 106 (3): 365–85. PMC 1224244. PMID 6323245.
- ^ Hua XH, Newport J (January 1998). "Identification of a preinitiation step in DNA replication that is independent of origin recognition complex and cdc6, but dependent on cdk2". Жасуша биологиясының журналы. 140 (2): 271–81. дои:10.1083/jcb.140.2.271. PMC 2132576. PMID 9442103.
- ^ Rowles A, Tada S, Blow JJ (June 1999). "Changes in association of the Xenopus origin recognition complex with chromatin on licensing of replication origins". Cell Science журналы. 112 (12): 2011–8. PMC 3605702. PMID 10341218.
- ^ а б c Li N, Zhai Y, Zhang Y, Li W, Yang M, Lei J, Tye BK, Gao N (August 2015). "Structure of the eukaryotic MCM complex at 3.8 Å". Табиғат. 524 (7564): 186–91. Бибкод:2015Natur.524..186L. дои:10.1038/nature14685. PMID 26222030. S2CID 4468690.
- ^ Noguchi Y, Yuan Z, Bai L, Schneider S, Zhao G, Stillman B, Speck C, Li H (November 2017). "Cryo-EM structure of Mcm2-7 double hexamer on DNA suggests a lagging-strand DNA extrusion model". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 114 (45): E9529–E9538. дои:10.1073/pnas.1712537114. PMC 5692578. PMID 29078375.
- ^ а б Dutta A, Bell SP (1997). "Initiation of DNA replication in eukaryotic cells". Жыл сайынғы жасуша мен даму биологиясына шолу. 13: 293–332. дои:10.1146/annurev.cellbio.13.1.293. PMID 9442876.
- ^ а б Labib K, Tercero JA, Diffley JF (June 2000). "Uninterrupted MCM2-7 function required for DNA replication fork progression". Ғылым. 288 (5471): 1643–7. Бибкод:2000Sci...288.1643L. дои:10.1126/science.288.5471.1643. PMID 10834843.
- ^ Schwacha A, Bell SP (November 2001). "Interactions between two catalytically distinct MCM subgroups are essential for coordinated ATP hydrolysis and DNA replication". Молекулалық жасуша. 8 (5): 1093–104. дои:10.1016/S1097-2765(01)00389-6. PMID 11741544.
- ^ Boyer PD (January 1993). "The binding change mechanism for ATP synthase--some probabilities and possibilities". Biochimica et Biofhysica Acta (BBA) - Биоэнергетика. 1140 (3): 215–50. дои:10.1016/0005-2728(93)90063-l. PMID 8417777.
- ^ Hingorani MM, Washington MT, Moore KC, Patel SS (May 1997). "The dTTPase mechanism of T7 DNA helicase resembles the binding change mechanism of the F1-ATPase". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 94 (10): 5012–7. Бибкод:1997PNAS...94.5012H. дои:10.1073/pnas.94.10.5012. PMC 24622. PMID 9144181.
- ^ Yan H, Merchant AM, Tye BK (November 1993). "Cell cycle-regulated nuclear localization of MCM2 and MCM3, which are required for the initiation of DNA synthesis at chromosomal replication origins in yeast". Гендер және даму. 7 (11): 2149–60. дои:10.1101/gad.7.11.2149. PMID 8224843.
- ^ Young MR, Suzuki K, Yan H, Gibson S, Tye BK (October 1997). "Nuclear accumulation of Saccharomyces cerevisiae Mcm3 is dependent on its nuclear localization sequence". Жасушаларға гендер. 2 (10): 631–43. дои:10.1046/j.1365-2443.1997.1510349.x. PMID 9427284.
- ^ Labib K, Diffley JF, Kearsey SE (November 1999). "G1-phase and B-type cyclins exclude the DNA-replication factor Mcm4 from the nucleus". Табиғи жасуша биологиясы. 1 (7): 415–22. дои:10.1038/15649. PMID 10559985. S2CID 23407351.
- ^ Lei M, Tye BK (April 2001). "Initiating DNA synthesis: from recruiting to activating the MCM complex". Cell Science журналы. 114 (Pt 8): 1447–54. PMID 11282021.
- ^ Leatherwood J (December 1998). "Emerging mechanisms of eukaryotic DNA replication initiation". Жасуша биологиясындағы қазіргі пікір. 10 (6): 742–8. дои:10.1016/S0955-0674(98)80117-8. PMID 9914182.
- ^ а б Mimura S, Takisawa H (October 1998). "Xenopus Cdc45-dependent loading of DNA polymerase alpha onto chromatin under the control of S-phase Cdk". EMBO журналы. 17 (19): 5699–707. дои:10.1093/emboj/17.19.5699. PMC 1170898. PMID 9755170.
- ^ а б Zou L, Stillman B (April 1998). "Formation of a preinitiation complex by S-phase cyclin CDK-dependent loading of Cdc45p onto chromatin". Ғылым. 280 (5363): 593–6. Бибкод:1998Sci...280..593Z. дои:10.1126/science.280.5363.593. PMID 9554851.
- ^ а б c Mimura S, Masuda T, Matsui T, Takisawa H (June 2000). "Central role for cdc45 in establishing an initiation complex of DNA replication in Xenopus egg extracts". Жасушаларға гендер. 5 (6): 439–52. дои:10.1046/j.1365-2443.2000.00340.x. PMID 10886370.
- ^ а б c Aparicio OM, Weinstein DM, Bell SP (October 1997). "Components and dynamics of DNA replication complexes in S. cerevisiae: redistribution of MCM proteins and Cdc45p during S phase". Ұяшық. 91 (1): 59–69. дои:10.1016/S0092-8674(01)80009-X. PMID 9335335. S2CID 10353164.
- ^ Tercero JA, Labib K, Diffley JF (May 2000). "DNA synthesis at individual replication forks requires the essential initiation factor Cdc45p". EMBO журналы. 19 (9): 2082–93. дои:10.1093/emboj/19.9.2082. PMC 305696. PMID 10790374.
- ^ Hennessy KM, Lee A, Chen E, Botstein D (June 1991). "A group of interacting yeast DNA replication genes". Гендер және даму. 5 (6): 958–69. дои:10.1101/gad.5.6.958. PMID 2044962.
- ^ Aparicio OM, Stout AM, Bell SP (August 1999). "Differential assembly of Cdc45p and DNA polymerases at early and late origins of DNA replication". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 96 (16): 9130–5. Бибкод:1999PNAS...96.9130A. дои:10.1073/pnas.96.16.9130. PMC 17744. PMID 10430907.
- ^ Zou L, Stillman B (May 2000). "Assembly of a complex containing Cdc45p, replication protein A, and Mcm2p at replication origins controlled by S-phase cyclin-dependent kinases and Cdc7p-Dbf4p kinase". Молекулалық және жасушалық биология. 20 (9): 3086–96. дои:10.1128/mcb.20.9.3086-3096.2000. PMC 85601. PMID 10757793.
- ^ а б Walter J, Newport J (April 2000). "Initiation of eukaryotic DNA replication: origin unwinding and sequential chromatin association of Cdc45, RPA, and DNA polymerase alpha". Молекулалық жасуша. 5 (4): 617–27. дои:10.1016/S1097-2765(00)80241-5. PMID 10882098.
- ^ а б c Gambus A, Jones RC, Sanchez-Diaz A, Kanemaki M, van Deursen F, Edmondson RD, Labib K (April 2006). "GINS maintains association of Cdc45 with MCM in replisome progression complexes at eukaryotic DNA replication forks". Табиғи жасуша биологиясы. 8 (4): 358–66. дои:10.1038/ncb1382. PMID 16531994. S2CID 21543095.
- ^ а б Kanemaki M, Sanchez-Diaz A, Gambus A, Labib K (June 2003). "Functional proteomic identification of DNA replication proteins by induced proteolysis in vivo". Табиғат. 423 (6941): 720–4. Бибкод:2003Natur.423..720K. дои:10.1038/nature01692. PMID 12768207. S2CID 4345091.
- ^ Makarova KS, Wolf YI, Mekhedov SL, Mirkin BG, Koonin EV (2005). "Ancestral paralogs and pseudoparalogs and their role in the emergence of the eukaryotic cell". Нуклеин қышқылдарын зерттеу. 33 (14): 4626–38. дои:10.1093/nar/gki775. PMC 1187821. PMID 16106042.
- ^ Moyer SE, Lewis PW, Botchan MR (July 2006). "Isolation of the Cdc45/Mcm2-7/GINS (CMG) complex, a candidate for the eukaryotic DNA replication fork helicase". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 103 (27): 10236–10241. Бибкод:2006PNAS..10310236M. дои:10.1073/pnas.0602400103. PMC 1482467. PMID 16798881.
- ^ Bochman ML, Schwacha A (July 2008). "The Mcm2-7 complex has in vitro helicase activity". Молекулалық жасуша. 31 (2): 287–93. дои:10.1016/j.molcel.2008.05.020. PMID 18657510.
- ^ Costa A, Ilves I, Tamberg N, Petojevic T, Nogales E, Botchan MR, Berger JM (April 2011). "The structural basis for MCM2-7 helicase activation by GINS and Cdc45". Табиғат құрылымы және молекулалық биология. 18 (4): 471–7. дои:10.1038/nsmb.2004. PMC 4184033. PMID 21378962.
- ^ Yuan Z, Bai L, Sun J, Georgescu R, Liu J, O'Donnell ME, Li H (March 2016). "Structure of the eukaryotic replicative CMG helicase suggests a pumpjack motion for translocation". Табиғат құрылымы және молекулалық биология. 23 (3): 217–24. дои:10.1038/nsmb.3170. PMC 4812828. PMID 26854665.
- ^ Homesley L, Lei M, Kawasaki Y, Sawyer S, Christensen T, Tye BK (April 2000). "Mcm10 and the MCM2-7 complex interact to initiate DNA synthesis and to release replication factors from origins". Гендер және даму. 14 (8): 913–26. дои:10.1101/gad.14.8.913 (белсенді емес 2020-09-01). PMC 316538. PMID 10783164.CS1 maint: DOI 2020 жылдың қыркүйегіндегі жағдай бойынша белсенді емес (сілтеме)
- ^ Christensen TW, Tye BK (маусым 2003). «Drosophila MCM10 пререпликация кешенінің мүшелерімен әрекеттеседі және хромосоманың дұрыс конденсациясы үшін қажет». Жасушаның молекулалық биологиясы. 14 (6): 2206–15. дои:10.1091 / mbc.e02-11-0706. PMC 194871. PMID 12808023.
- ^ Ли С, Лиачко I, Бутен Р, Келман З, Тай Б.К. (қаңтар 2010). «Полимеразды альфа мен MCM геликазаны үйлестірудің баламалы механизмдері». Молекулалық және жасушалық биология. 30 (2): 423–35. дои:10.1128 / MCB.01240-09. PMC 2798462. PMID 19917723.
- ^ ван Дурсен Ф, Сенгупта С, Де Пикколи Г, Санчес-Диас А, Лабиб К (мамыр 2012). «Mcm10 репликация шыққан кезде жүктелген ДНҚ-геликазамен байланысады және оны белсендірудің жаңа қадамын анықтайды». EMBO журналы. 31 (9): 2195–206. дои:10.1038 / emboj.2012.69. PMC 3343467. PMID 22433841.
- ^ Масаи Х, Сато Н, Такеда Т, Арай К (желтоқсан 1999). «ДНҚ репликациясының молекулалық қосқышы ретінде CDC7 киназа кешені». Биологиядағы шекаралар. 4 (1-3): D834-40. дои:10.2741 / masai. PMID 10577390.
- ^ Jiang W, Wells NJ, Hunter T (мамыр 1999). «HsCdc6 фосфорлануының Cdk арқылы ДНҚ репликациясының көп сатылы реттелуі». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 96 (11): 6193–8. Бибкод:1999 PNAS ... 96.6193J. дои:10.1073 / pnas.96.11.6193. PMC 26858. PMID 10339564.
- ^ а б Jiang W, McDonald D, Hope TJ, Hunter T (қазан 1999). «Сүтқоректілердің Cdc7-Dbf4 ақуыздық киназа кешені ДНҚ репликациясын бастау үшін өте маңызды». EMBO журналы. 18 (20): 5703–13. дои:10.1093 / emboj / 18.20.5703. PMC 1171637. PMID 10523313.
- ^ Кумагай Х, Сато Н, Ямада М, Махони Д, Сегеззи В, Лис Е, Арай К, Масаи Н (шілде 1999). «Жасуша циклімен реттелетін өсу және жасушалық циклмен реттелетін жаңа протеин, ASK, адамның Cdc7-ге байланысты киназасын белсендіреді және сүтқоректілердің жасушаларында G1 / S ауысуы үшін өте маңызды». Молекулалық және жасушалық биология. 19 (7): 5083–95. дои:10.1128 / MCB.19.7.5083. PMC 84351. PMID 10373557.
- ^ Lei M, Kawasaki Y, Young MR, Kihara M, Sugino A, Tye BK (желтоқсан 1997). «Mcm2 - ДНҚ синтезі басталған кезде Cdc7-Dbf4 реттелуінің мақсаты». Гендер және даму. 11 (24): 3365–74. дои:10.1101 / gad.11.24.3365. PMC 316824. PMID 9407029.
- ^ Hardy CF, Dryga O, Seematter S, Pahl PM, Sclafani RA (сәуір 1997). «mcm5 / cdc46-bob1 S фаза активаторы Cdc7p талаптарын айналып өтеді». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 94 (7): 3151–5. Бибкод:1997 PNAS ... 94.3151H. дои:10.1073 / pnas.94.7.3151. PMC 20337. PMID 9096361.
- ^ Kamimura Y, Tak YS, Sugino A, Araki H (сәуір 2001). «Cdc45 (Sld4) -мен әрекеттесетін Sld3, Saccharomyces cerevisiae-де хромосомалық ДНҚ репликациясының функциялары». EMBO журналы. 20 (8): 2097–107. дои:10.1093 / emboj / 20.8.2097. PMC 125422. PMID 11296242.
- ^ Канемаки М, Лабиб К (сәуір 2006). «Эукариоттық ДНҚ репликациясының шанышқыларын құру және прогрессия кезінде Sld3 және GINS үшін ерекше рөлдер». EMBO журналы. 25 (8): 1753–63. дои:10.1038 / sj.emboj.7601063. PMC 1440835. PMID 16601689.
- ^ Масумото Х, Сугино А, Араки Н (сәуір 2000). «Dpb11 альфа және эпсилон ДНҚ-полимеразалары мен бүршік жасайтын ашытқының автономды репликацияланатын дәйектілік аймағы арасындағы байланысты бақылайды». Молекулалық және жасушалық биология. 20 (8): 2809–17. дои:10.1128 / mcb.20.8.2809-2817.2000. PMC 85497. PMID 10733584.
- ^ Araki H, Leem SH, Phongdara A, Sugino A (желтоқсан 1995). «Saccharomyces cerevisiae құрамындағы ДНҚ-полимераза II-мен (эпсилон) өзара әрекеттесетін Dpb11, S-фазалық прогрессияда және жасушалық циклды бақылау нүктесінде қосарланған рөл атқарады». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 92 (25): 11791–5. дои:10.1073 / pnas.92.25.11791. PMC 40488. PMID 8524850.
- ^ Glover JN, Williams RS, Lee MS (қараша 2004). «BRCT қайталанулары мен фосфопротеиндер арасындағы өзара әрекеттесу: екіге оралған». Биохимия ғылымдарының тенденциялары. 29 (11): 579–85. дои:10.1016 / j.tibs.2004.09.010. PMID 15501676.
- ^ Масумото Х, Мурамацу С, Камимура Ю, Араки Н (ақпан 2002). «Snd-тәуелді Sld2 фосфорлануы, ашытқыда хромосомалық ДНҚ репликациясы үшін маңызды». Табиғат. 415 (6872): 651–5. Бибкод:2002 ж. 415..651М. дои:10.1038 / табиғат713. PMID 11807498. S2CID 4300863.
- ^ Такаяма Y, Камимура Ю, Окава М, Мурамацу С, Сугино А, Араки Х (мамыр 2003). «GINS, жаңа ашытқыдағы хромосомалық ДНҚ репликациясы үшін қажет жаңа мульти протеин кешені». Гендер және даму. 17 (9): 1153–65. дои:10.1101 / gad.1065903. PMC 196052. PMID 12730134.
- ^ Лабиб К, Гамбус А (маусым 2007). «ДНҚ репликациясының айырларындағы GINS кешені үшін маңызды рөл». Жасуша биологиясының тенденциялары. 17 (6): 271–8. дои:10.1016 / j.tb.2007.04.002. PMID 17467990.
- ^ Muramatsu S, Hirai K, Tak YS, Kamimura Y, Araki H (наурыз 2010). «Dpb11, Sld2, Pol (эпсилон} және GINS репликациясы ақуыздары арасындағы ашытқыдағы репликация белоктарының арасындағы CDK тәуелді кешенді түзіліс». Гендер және даму. 24 (6): 602–12. дои:10.1101 / gad.1883410. PMC 2841337. PMID 20231317.
- ^ Леман И.Р., Бессман М.Дж., Симмс Э.С., Корнберг А (шілде 1958). «Дезоксирибонуклеин қышқылының ферментативті синтезі. I. Субстраттарды дайындау және ферментті ішек таяқшасынан ішінара тазарту». Биологиялық химия журналы. 233 (1): 163–70. PMID 13563462.
- ^ Алани Е, Трезер Р, Гриффит Дж.Д., Колоднер РД (қыркүйек 1992). «ДНҚ байланыстыратын және спиральды алмасу ынталандыру қасиеттерін сипаттау y-RPA, ашытқы бір тізбекті-ДНҚ байланыстыратын ақуыз». Молекулалық биология журналы. 227 (1): 54–71. дои:10.1016/0022-2836(92)90681-9. PMID 1522601.
- ^ Гулян М, Ричардс Ш., Херд Дж., Бигсби Б.М. (қазан 1990). «Тазартылған сүтқоректілердің ақуыздарымен ДНҚ синтезі». Биологиялық химия журналы. 265 (30): 18461–71. PMID 2170412.
- ^ McCulloch SD, Kunkel TA (қаңтар 2008). «Эукариоттық репликативті және транслезиялық синтез полимеразаларымен ДНҚ синтезінің сенімділігі». Жасушаларды зерттеу. 18 (1): 148–61. дои:10.1038 / кр.2008.4. PMC 3639319. PMID 18166979.
- ^ Pursell ZF, Isoz I, Lundström EB, Johansson E, Kunkel TA (шілде 2007). «ДНҚ-полимераз эпсилоны ашытқы ДНҚ-ның жетекші репликациясына қатысады». Ғылым. 317 (5834): 127–30. Бибкод:2007Sci ... 317..127P. дои:10.1126 / ғылым.1144067. PMC 2233713. PMID 17615360.
- ^ а б c г. e Уотсон Дж, Бейкер Т, Белл С, Ганн А, Левин М, Лосик Р, Геннің молекулалық биологиясы 6-шығарылым, Pearson Education Inc, 2008 ж. ISBN 080539592X
- ^ Waga S, Bauer G, Stillman B (сәуір 1994). «SV40 ДНҚ-ның толық репликациясын тазартылған репликация факторларымен қалпына келтіру». Биологиялық химия журналы. 269 (14): 10923–34. PMID 8144677.
- ^ Garg P, Stith CM, Sabouri N, Johansson E, Burgers PM (қараша 2004). «ДНҚ-полимераз дельтасында бос жүру ДНҚ-ның артта қалу репликациясы кезінде байлаулы никті сақтайды». Гендер және даму. 18 (22): 2764–73. дои:10.1101 / gad.1252304. PMC 528896. PMID 15520275.
- ^ Burgers PM (ақпан 2009). «Эукариоттық ДНҚ репликациясының ашасындағы полимераз динамикасы». Биологиялық химия журналы. 284 (7): 4041–5. дои:10.1074 / jbc.R800062200. PMC 2640984. PMID 18835809.
- ^ Jin YH, Ayyagari R, Resnick MA, Gordenin DA, Burgers PM (қаңтар 2003). «Ашытқыдағы оказаки фрагментінің жетілуі. II. Пол дельтаның полимераза мен 3'-5'-экзонуклеазалық белсенділігі арасындағы байланысатын ник құрудағы ынтымақтастық». Биологиялық химия журналы. 278 (3): 1626–33. дои:10.1074 / jbc.M209803200. PMID 12424237.
- ^ Sogo JM, Lopes M, Foiani M (шілде 2002). «Бақылау пунктінің ақауларына байланысты тоқтап қалған репликация шанышқыларындағы шанышқылардың өзгеруі және ssDNA жинақталуы». Ғылым. 297 (5581): 599–602. Бибкод:2002Sci ... 297..599S. дои:10.1126 / ғылым.1074023. PMID 12142537. S2CID 33502697.
- ^ Моррисон А, Араки Х, Кларк А.Б., Хаматаке Р.К., Сугино А (қыркүйек 1990). «S. cerevisiae-де үшінші маңызды ДНҚ-полимераза». Ұяшық. 62 (6): 1143–51. дои:10.1016 / 0092-8674 (90) 90391-Q. PMID 2169349. S2CID 29672985.
- ^ Waga S, Stillman B (мамыр 1994). «SV40 ДНҚ репликациясының in vitro қалпына келтірілуімен анықталған ДНҚ репликациясы шанышқысының анатомиясы». Табиғат. 369 (6477): 207–12. Бибкод:1994 ж.36..207W. дои:10.1038 / 369207a0. PMID 7910375. S2CID 4351628.
- ^ Цуримото Т, Стиллман Б (қаңтар 1991). «SV40 ДНҚ-ның экстракорпоральды репликациясы үшін қажетті репликация факторлары. II. Жетекші және артта қалған тізбек синтезі басталған кезде альфа мен дельтаның ДНҚ-сының ауысуы». Биологиялық химия журналы. 266 (3): 1961–8. PMID 1671046.
- ^ Barry ER, Bell SD (желтоқсан 2006). «Археядағы ДНҚ репликациясы». Микробиология және молекулалық биологияға шолу. 70 (4): 876–87. дои:10.1128 / MMBR.00029-06. PMC 1698513. PMID 17158702.
- ^ Берг Дж.М., Тимочко Дж.Л., Страйер Л (2003). Биохимия. Гейдельберг / Берлин: Шпрингер.
- ^ а б Джонсон RE, Klassen R, Prakash L, Prakash S (шілде 2015). «ДНҚ полимеразының басты рөлі - жетекші де, артта қалған ДНҚ тізбегін де көбейтуде». Молекулалық жасуша. 59 (2): 163–175. дои:10.1016 / j.molcel.2015.05.038. PMC 4517859. PMID 26145172.
- ^ Byun TS, Pacek M, Yee MC, Walter JC, Cimprich KA (мамыр 2005). «MCM геликаза мен ДНҚ-полимеразаның белсенділігін функционалды түрде ажырату ATR-тәуелді бақылау нүктесін белсендіреді». Гендер және даму. 19 (9): 1040–52. дои:10.1101 / gad.1301205. PMC 1091739. PMID 15833913.
- ^ а б Remus D, Beuron F, Tolun G, Griffith JD, Morris EP, Diffley JF (қараша 2009). «ДНҚ репликациясының шығу тегі лицензиялану кезінде ДНҚ айналасында Mcm2-7 қос гексамерлерін концентрациялы түрде жүктеу». Ұяшық. 139 (4): 719–30. дои:10.1016 / j.cell.2009.10.015. PMC 2804858. PMID 19896182.
- ^ Evrin C, Clarke P, Zech J, Lurz R, Sun J, Uhle S, Li H, Stillman B, Speck C (желтоқсан 2009). «Эукариотты ДНҚ репликациясын лицензиялау кезінде қос гексамерлі MCM2-7 кешені бастапқы ДНҚ-ға жүктеледі». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 106 (48): 20240–5. Бибкод:2009PNAS..10620240E. дои:10.1073 / pnas.0911500106. PMC 2787165. PMID 19910535.
- ^ а б Moyer SE, Lewis PW, Botchan MR (шілде 2006). «Cdc45 / Mcm2-7 / GINS (CMG) кешенін оқшаулау, эукариоттық ДНҚ репликациясының шанышқы геликазасына үміткер». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 103 (27): 10236–10241. Бибкод:2006PNAS..10310236M. дои:10.1073 / pnas.0602400103. PMC 1482467. PMID 16798881.
- ^ Лабиб К (маусым 2010). «Cdc7 және циклинге тәуелді киназдар эукариоттық жасушаларда хромосомалардың репликациясының иницирациясын қалай қоздырады?». Гендер және даму. 24 (12): 1208–19. дои:10.1101 / gad.1933010. PMC 2885657. PMID 20551170.
- ^ Pacek M, Walter JC (қыркүйек 2004). «Эукариоттық ДНҚ репликациясы кезінде хромосоманың таралуындағы MCM7 және Cdc45-ке қойылатын талап». EMBO журналы. 23 (18): 3667–76. дои:10.1038 / sj.emboj.7600369. PMC 517609. PMID 15329670.
- ^ Яо Нью-Йорк, О'Доннелл М (маусым 2010). «SnapShot: ауыстырғыш». Ұяшық. 141 (6): 1088–1088.e1. дои:10.1016 / j.cell.2010.05.042. PMC 4007198. PMID 20550941.
- ^ Коста А, Ильвес I, Тамберг Н, Петоевич Т, Ногалес Е, Ботчан М.Р., Бергер Дж.М. (сәуір 2011). «MCM2-7 геликазаны GINS және Cdc45 активациясының құрылымдық негіздері». Табиғат құрылымы және молекулалық биология. 18 (4): 471–7. дои:10.1038 / nsmb.2004. PMC 4184033. PMID 21378962.
- ^ Bermudez VP, Farina A, Tappin I, Hurwitz J (наурыз 2010). «ДНҚ репликациясына адамның біртектілік факторының Ctf4 / AND-1 әсер етуі». Биологиялық химия журналы. 285 (13): 9493–505. дои:10.1074 / jbc.M109.093609. PMC 2843200. PMID 20089864.
- ^ Zhu W, Ukomadu C, Jha S, Senga T, Dhar SK, Wohlschlegel JA, Nutt LK, Kornbluth S, Dutta A (қыркүйек 2007). «Mcm10 және And-1 / CTF4 ДНҚ репликациясын бастау үшін ДНҚ-полимераза альфасын хроматинге қосады». Гендер және даму. 21 (18): 2288–99. дои:10.1101 / gad.1585607. PMC 1973143. PMID 17761813.
- ^ Lou H, Komata M, Katou Y, Guan Z, Reis CC, Budd M, Shirahige K, Campbell JL (қазан 2008). «Mrc1 және ДНҚ-полимераза эпсилоны ДНҚ репликациясы мен S фазасының бақылау нүктесін байланыстыруда бірге жұмыс істейді». Молекулалық жасуша. 32 (1): 106–17. дои:10.1016 / j.molcel.2008.08.020. PMC 2699584. PMID 18851837.
- ^ Petermann E, Helleday T, Caldecott KW (маусым 2008). «Клазпин адам клеткаларындағы шанышқының қалыпты репликациялануына ықпал етеді». Жасушаның молекулалық биологиясы. 19 (6): 2373–8. дои:10.1091 / mbc.E07-10-1035. PMC 2397295. PMID 18353973.
- ^ Bravo R, Frank R, Blundell PA, Macdonald-Bravo H (1987). «Циклин / ПКНА - ДНҚ полимераза-дельтаның көмекші ақуызы». Табиғат. 326 (6112): 515–7. Бибкод:1987 ж.36..515B. дои:10.1038 / 326515a0. PMID 2882423. S2CID 4344147.
- ^ Прелих Г, Тан К.К., Костура М, Мэтьюз М.Б, Со А.Г., Дауни К.М., Стиллман Б (1987). «Пролиферацияланатын жасушалық ядролық антигеннің және ДНҚ полимераза-дельта көмекші ақуызының функционалды сәйкестігі». Табиғат. 326 (6112): 517–20. Бибкод:1987 ж.326..517Б. дои:10.1038 / 326517a0. PMID 2882424. S2CID 4345171.
- ^ Молдова GL, Pfander B, Jentsch S (мамыр 2007). «PCNA, репликация шанышқының маэстрасы». Ұяшық. 129 (4): 665–79. дои:10.1016 / j.cell.2007.05.003. PMID 17512402. S2CID 3547069.
- ^ Cai J, Yao N, Gibbs E, Finkelstein J, Phillips B, O'Donnell M, Hurwitz J (қыркүйек 1998). «Адамның репликация коэффициентімен катализденетін АТФ гидролизі көптеген суббірліктердің қатысуын қажет етеді». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 95 (20): 11607–12. Бибкод:1998 PNAS ... 9511607C. дои:10.1073 / pnas.95.20.11607. PMC 21688. PMID 9751713.
- ^ Цуримото Т, Стиллман Б (қаңтар 1991). «SV40 ДНҚ-ның экстракорпоральды репликациясына қажет репликация факторлары. I. Эукариотты ДНҚ полимеразалары мен олардың қосымша ақуыздарының праймер-шаблон байланысын ДНҚ құрылымына тән тану». Биологиялық химия журналы. 266 (3): 1950–60. PMID 1671045.
- ^ Podust LM, Podust VN, Sogo JM, Hübscher U (маусым 1995). «Сүтқоректілердің ДНҚ полимеразының көмекші ақуыздары: репликация коэффициентінің анализі, С-катализденген пролиферацияланатын жасуша ядролық антигені дөңгелек екі тізбекті ДНҚ-ға тиеу». Молекулалық және жасушалық биология. 15 (6): 3072–81. дои:10.1128 / MCB.15.6.3072. PMC 230538. PMID 7760803.
- ^ Чжан Г, Гиббс Е, Келман З, О'Доннелл М, Хурвит Дж (наурыз 1999). «Адамның репликация коэффициенті мен адамның көбеюіндегі жасушалық ядролық антигеннің өзара әрекеттесуі туралы зерттеулер». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 96 (5): 1869–74. Бибкод:1999 PNAS ... 96.1869Z. дои:10.1073 / pnas.96.5.1869. PMC 26703. PMID 10051561.
- ^ а б Яо Нью-Йорк, Джонсон А, Боуман Г.Д., Куриян Дж, О'Доннелл М (маусым 2006). «Репликация коэффициенті арқылы жасушалардың ядролық антигенді қысқышын көбейту механизмі». Биологиялық химия журналы. 281 (25): 17528–39. дои:10.1074 / jbc.M601273200. PMID 16608854.
- ^ а б c Сабатинос, SA (2010). «Тоқтап қалған реплика шанышқысын қалпына келтіру». Табиғи табиғат туралы білім. 3 (9): 31.
- ^ а б Rothstein R, Michel B, Gangloff S (қаңтар 2000). «Репликациялық шанышқыны кідірту және рекомбинациялау немесе» үзіліске жол беру"". Гендер және даму. 14 (1): 1–10. PMID 10640269.
- ^ Bastia D, Zzaman S, Krings G, Saxena M, Peng X, Greenberg MM (қыркүйек 2008). «Жылжымалы геликазаның Тус-делдалды полярлы ұсталуынан анықталған репликацияны тоқтату механизмі». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 105 (35): 12831–6. Бибкод:2008PNAS..10512831B. дои:10.1073 / pnas.0805898105. PMC 2529109. PMID 18708526.
- ^ Репликация фабрикалары, ПавелХозак, Питер Р.Кук, Жасуша биологиясының тенденциялары 4 том 2 шығарылым; Тәжірибелі, DOI
- ^ McGarry TJ, Kirschner MW (маусым 1998). «Митоз кезінде ДНҚ репликациясының ингибиторы - геминин деградацияға ұшырайды». Ұяшық. 93 (6): 1043–53. дои:10.1016 / S0092-8674 (00) 81209-X. PMID 9635433. S2CID 235485.
- ^ де Клейн А, Муйтженс М, Ван Ос Р, Верховен Ю, Смит Б, Карр А.М., Леман А.Р., Хоймейкерлер JH (сәуір 2000). «ATR генінің жасушалық циклінің мақсатты түрде бұзылуы тышқандарда ерте эмбриональды өлімге әкеледі». Қазіргі биология. 10 (8): 479–82. дои:10.1016 / S0960-9822 (00) 00447-4. PMID 10801416. S2CID 15401622.
- ^ Cortez D, Guntuku S, Qin J, Elledge SJ (қараша 2001). «ATR және ATRIP: бақылау-өткізу пунктіндегі серіктестер». Ғылым. 294 (5547): 1713–6. Бибкод:2001Sci ... 294.1713C. дои:10.1126 / ғылым.1065521. PMID 11721054. S2CID 32810119.
- ^ Dart DA, Adams KE, Akerman I, Lakin ND (сәуір 2004). «S-фаза кезінде хроматинге ATR киназа клеткалық циклін қабылдау». Биологиялық химия журналы. 279 (16): 16433–40. дои:10.1074 / jbc.M314212200. PMID 14871897.
- ^ Ball HL, Myers JS, Cortez D (мамыр 2005). «ATRIP репликациясының ақуызымен байланысуы A-бір тізбекті ДНҚ ATR-ATRIP локализациясына ықпал етеді, бірақ Chk1 фосфорлану үшін бөлінеді». Жасушаның молекулалық биологиясы. 16 (5): 2372–81. дои:10.1091 / mbc.E04-11-1006. PMC 1087242. PMID 15743907.
- ^ Bermudez VP, Lindsey-Boltz LA, Cesare AJ, Maniwa Y, Griffith JD, Hurwitz J, Sancar A (ақпан 2003). «9-1-1 бақылау-өткізу пунктінің кешенін ДНҚ-ға жүктеу бақылау нүктесінің қысқыш-жүктегіші арқылы hRad17-репликация коэффициенті C in vitro». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 100 (4): 1633–8. Бибкод:2003PNAS..100.1633B. дои:10.1073 / pnas.0437927100. PMC 149884. PMID 12578958.
- ^ Zou L, Cortez D, Elledge SJ (қаңтар 2002). «Рад9 комплекстерінің хроматинге Rad17 тәуелді жүктемесі бойынша ATR субстратты таңдауды реттеу». Гендер және даму. 16 (2): 198–208. дои:10.1101 / gad.950302. PMC 155323. PMID 11799063.
- ^ Кумагай А, Дэнфи В.Г. (қазан 2000). «Ксенпиннің жұмыртқа сығындыларындағы ДНҚ репликациясының бақылау нүктесінің реакциясы кезінде Chk1 активациясы үшін қажетті жаңа ақуыз». Молекулалық жасуша. 6 (4): 839–49. дои:10.1016 / S1097-2765 (05) 00092-4. PMID 11090622.
- ^ Кумагай А, Дэнфи ВГ (ақпан 2003). «Класпиндегі қайталанған фосфопептидтік мотивтер Chk1-нің реттелетін байланысын қамтамасыз етеді» (PDF). Табиғи жасуша биологиясы. 5 (2): 161–5. дои:10.1038 / ncb921. PMID 12545175. S2CID 29331203.
- ^ Miao H, Seiler JA, Burhans WC (ақпан 2003). «Chk1-тәуелді ішкі және UVC сәулеленуіне байланысты бақылау-өткізу пункттерімен репликацияның жасушалық және SV40 вирусының шығу тегі». Биологиялық химия журналы. 278 (6): 4295–304. дои:10.1074 / jbc.M204264200. PMID 12424256.
- ^ Бар-Зив Р, Войчек Ю, Баркай Н (қыркүйек 2016). «ДНҚ репликациясы кезіндегі хроматин динамикасы». Геномды зерттеу. 26 (9): 1245–56. дои:10.1101 / гр.201244.115. PMC 5052047. PMID 27225843.
- ^ Luger K, Mäder AW, Richmond RK, Sargent DF, Richmond TJ (қыркүйек 1997). «Нуклеосома ядросы бөлшегінің кристалдық құрылымы 2,8 А ажыратымдылықта». Табиғат. 389 (6648): 251–60. Бибкод:1997 ж.389..251L. дои:10.1038/38444. PMID 9305837. S2CID 4328827.
- ^ Wittmeyer J, Joss L, Formosa T (шілде 1999). «Saccharomyces cerevisiae-дің Spt16 және Pob3 ядролық, хроматинмен байланысқан және ДНҚ-полимераз альфа-мен копирирленген маңызды, мол гетеродимер құрайды». Биохимия. 38 (28): 8961–71. дои:10.1021 / bi982851d. PMID 10413469.
- ^ Wittmeyer J, Formosa T (шілде 1997). «Saccharomyces cerevisiae ДНҚ-полимераз альфа-каталитикалық суббірлігі Cdc68 / Spt16 және HMG1 тәрізді ақуызға ұқсас Pob3-пен әрекеттеседі». Молекулалық және жасушалық биология. 17 (7): 4178–90. дои:10.1128 / MCB.17.7.4178. PMC 232271. PMID 9199353.
- ^ Xin H, Takahata S, Blanksma M, McCullough L, Stillman DJ, Formosa T (тамыз 2009). «yFACT H2A-H2B орын ауыстыруынсыз нуклеосомалық ДНҚ-ның ғаламдық қол жетімділігін тудырады». Молекулалық жасуша. 35 (3): 365–76. дои:10.1016 / j.molcel.2009.06.024. PMC 2748400. PMID 19683499.
- ^ Грот А, Корпет А, Кук АЖ, Рош Д, Бартек Дж, Лукас Дж, Алмузни Г (желтоқсан 2007). «Гистонға сұраныс пен ұсыныс арқылы реплика форкасының прогрессиясын реттеу». Ғылым. 318 (5858): 1928–31. Бибкод:2007Sci ... 318.1928G. дои:10.1126 / ғылым.1148992. PMID 18096807. S2CID 22350778.
- ^ Daganzo SM, Erzberger JP, Lam WM, Skordalakes E, Zhang R, Franco AA, Brill SJ, Adams PD, Berger JM, Kaufman PD (желтоқсан 2003). «Asf1 гистонды тұндыру ақуызының сақталған ядросының құрылымы және қызметі». Қазіргі биология. 13 (24): 2148–58. дои:10.1016 / j.cub.2003.11.027. PMID 14680630. S2CID 15164132.
- ^ Voichek Y, Bar-Ziv R, Barkai N (наурыз 2016). «ДНҚ репликациясы кезіндегі экспрессия гомеостазы». Ғылым. 351 (6277): 1087–90. Бибкод:2016Sci ... 351.1087V. дои:10.1126 / science.aad1162. PMID 26941319. S2CID 32751800.
- ^ Stillman B (мамыр 1986). «SV40 ДНҚ-ның in vitro репликациясы кезіндегі хроматин жиынтығы». Ұяшық. 45 (4): 555–65. дои:10.1016/0092-8674(86)90287-4. PMID 3011272. S2CID 21212160.
- ^ Шибахара К, Стиллман Б (ақпан 1999). «РНҚ-ның репликацияға тәуелді таңбалауы хроматиннің CAF-1 байланыстырылған тұқым қуалауын жеңілдетеді». Ұяшық. 96 (4): 575–85. дои:10.1016 / S0092-8674 (00) 80661-3. PMID 10052459. S2CID 13912324.
- ^ Rolef Ben-Shahar T, Castillo AG, Osborne MJ, Borden KL, Kornblatt J, Verreault A (желтоқсан 2009). «PCNA өзара әрекеттесуінің екі пептидтері хроматинді жинау фактор-1 функциясына ықпал етеді». Молекулалық және жасушалық биология. 29 (24): 6353–65. дои:10.1128 / MCB.01051-09. PMC 2786881. PMID 19822659.
- ^ Хуанг С, Чжоу Х, Кацманн Д, Хохстрассер М, Атанасова Е, Чжан З (қыркүйек 2005). «Rtt106p - гетерохроматинді-тыныштандыруға қатысатын гистон шапероны». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 102 (38): 13410–5. Бибкод:2005 PNAS..10213410H. дои:10.1073 / pnas.0506176102. PMC 1224646. PMID 16157874.
- ^ Ito T, Tyler JK, Bulger M, Kobayashi R, Kadonaga JT (қазан 1996). «Drosophila melanogaster-ден нуклеоплазмин тәрізді ақуызбен ATP жеңілдетілген хроматинді құрастыру». Биологиялық химия журналы. 271 (40): 25041–8. дои:10.1074 / jbc.271.40.25041. PMID 8798787.
- ^ Gasser R, Koller T, Sogo JM (мамыр 1996). «Репликация шанышқысындағы нуклеосомалардың тұрақтылығы». Молекулалық биология журналы. 258 (2): 224–39. дои:10.1006 / jmbi.1996.0245. PMID 8627621.
- ^ Меселсон М, Штал ФВ (шілде 1958). «ДНҚ-ның ішек таяқшасындағы репликациясы». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 44 (7): 671–82. Бибкод:1958 PNAS ... 44..671M. дои:10.1073 / pnas.44.7.671. PMC 528642. PMID 16590258.
- ^ Bell SP, Kaguni JM (маусым 2013). «Репликацияның хромосомалық бастауларында геликаза жүктемесі». Биологиядағы суық көктем айлағының болашағы. 5 (6): a010124. дои:10.1101 / cshperspect.a010124. PMC 3660832. PMID 23613349.

