Перовскит (құрылым) - Perovskite (structure)

A перовскит а бар кез-келген материал болып табылады кристалдық құрылым ұқсас перовскит деп аталатын минерал, ол тұрады кальций титан оксиді (CaTiO3).[2] Минерал алғаш рет Орал таулары Ресей арқылы Густав Роуз 1839 ж. және орыс минералогының есімімен аталған Перовский (1792–1856). Перовскит қосылыстарының жалпы химиялық формуласы - ABX3, мұндағы 'А' және 'B' екі катиондар, көбінесе әртүрлі мөлшерде, ал X - ан анион екі катионмен байланысатын (жиі оксид). 'A' атомдары, әдетте, 'B' атомдарынан үлкенірек. Идеал кубтық құрылымда В бар катион қоршауда 6 рет үйлестіру октаэдр туралы аниондар және катион 12 есе кубоктаэдрлік үйлестіру.
Перовскиттер құрылымдық отбасылардың бірі ретінде кең қасиеттерге, қолданылуларға және маңыздылыққа ие көптеген қосылыстарда кездеседі.[3] Мұндай құрылымды табиғи қосылыстар перовскит, лопарит, және силикатты перовскит бридгманит.[2][4] Ашылғаннан бері перовскитті күн батареялары құрамында, бар метиламмоний қорғасын галоид 2009 жылы перовскиттік материалдарға ғылыми қызығушылық айтарлықтай болды.[5]
Құрылым
Перовскит құрылымдарын көптеген адамдар қабылдайды оксидтер АВО химиялық формуласы бар3. Идеалданған форма - бұл кубтық құрылым (ғарыш тобы Pm3м, жоқ. 221) сирек кездеседі. The ортомомиялық (мысалы, ғарыш тобы Пнма, жоқ. 62, немесе Amm2, жоқ. 68) және төртбұрышты (мысалы, ғарыш тобы I4 / mcm, жоқ. 140 немесе P4mm, жоқ. 99) фазалар - кең таралған кубтық емес нұсқалар. Перовскит құрылымы CaTiO атымен аталғанымен3, бұл минерал идеализацияланбаған форманы құрайды. SrTiO3 және CaRbF3 кубтық перовскиттердің мысалдары болып табылады. Барий титанаты ромбоведральды қабылдай алатын перовскиттің мысалы болып табылады (ғарыш тобы R3м, жоқ. 160), температураға байланысты орторомбиялық, тетрагоналды және кубтық формалар.[6]
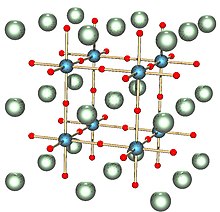
Идеалдандырылған кубта ұяшық осындай қосылыстың «А» типті атомы кубтың бұрышында (0, 0, 0), ал «В» атомы дененің центрінде орналасады (1/2, 1/2, 1/2) және оттегі атомдары (1/2, 1/2, 0), (1/2, 0, 1/2) және (0, 1/2, 1/2) орталықтандырылған позицияларда отырады. Оң жақтағы диаграммада эквивалентті бірлік ұяшығының шеттері A кубтық бұрышта, дене ортасында B, ал O центрге бағытталған позицияларда көрсетілген.
Катионды жұптаудың үш жалпы санаты мүмкін: A2+B4+X2−3немесе 2: 4 перовскиттер; A3+B3+X2−3, немесе 3: 3 перовскиттер; және А+B5+X2−3, немесе 1: 5 перовскиттер.
Текше құрылымының тұрақтылығына қатысты ион мөлшерінің салыстырмалы талаптары өте қатал, сондықтан бұралаңдау мен бұрмалану бірнеше төменгі симметриялы бұрмаланған нұсқаларды тудыруы мүмкін, онда А катиондарының, В катиондарының немесе екеуінің координациялық сандары азаяды. БО-ны еңкейту6 октаэдр кіші катионның координациясын 12-ден 8-ге дейін төмендетеді, керісінше, кіші В катионын оның октаэдрінде центрден тыс бағыттау тұрақты байланыс үлгісіне қол жеткізуге мүмкіндік береді. Алынған электрлік диполь меншік үшін жауап береді электр қуаты және BaTiO сияқты перовскиттер көрсеткен3 осы қалыпта бұрмалайды.
Күрделі перовскит құрылымдарында екі түрлі В-катионы бар. Бұл реттелген және ретсіз нұсқалардың мүмкіндігіне әкеледі.
Қабатты перовскиттер
Перовскиттер қабаттасып құрылымдалуы мүмкін ABO
3 интрузивті материалдың жұқа парақтарымен бөлінген құрылым. Интрузияның химиялық құрамына негізделген интрузиялардың әртүрлі формалары:[7]
- Aurivillius фазасы: еніп жатқан қабат [Би
2O
2]2+ ион, әрқайсысында кездеседі n ABO
3 жалпы химиялық формулаға әкелетін қабаттар [Би
2O
2]-A
(n−1)B
2O
7. Олардың тотықты ион өткізгіштік қасиеттерін алғаш рет 1970 жылдары Такахаши және басқалар тапқан және олар содан бері осы мақсатта қолданылып келеді.[8] - Дион − Джейкобсон фазасы: енетін қабат сілтілік металдан (М) тұрады n ABO
3 ретінде жалпы формуланы бере отырып, қабаттар М+
A
(n−1)B
nO
(3n+1) - Радлсден-Поппер фазасы: ең қарапайым фазалар, енетін қабат әрқайсысының арасында пайда болады (n = 1) немесе екі (n = 2) қабаттар ABO
3 тор. Радлсден − Поппер фазалары элементтердің атомдық радиустары жағынан перовскиттерге ұқсас қатынасқа ие, олардың А мөлшері үлкен (мысалы, La[9] немесе Sr[10]) B ионының өтпелі металдан (мысалы, Mn,[9] Co[11] немесе Ni[12]).
Жіңішке фильмдер

Перовскиттерді эпитаксиальды жұқа қабықшалар ретінде басқа перовскиттердің үстіне қоюға болады,[13] сияқты техниканы қолдана отырып импульсті лазерлік тұндыру және молекулалық-сәулелік эпитаксия. Бұл пленкалар жұп нанометр немесе бір өлшемді ұяшық сияқты кішкентай болуы мүмкін.[14] Фильм мен субстрат арасындағы интерфейстерде жақсы анықталған және ерекше құрылымдар жаңа типтік қасиеттер туындауы мүмкін интерфейсті жобалау үшін қолданыла алады.[15] Бұл субстрат пен пленка арасындағы сәйкессіздіктен, оттегі октаэдрлік айналуының өзгеруінен, композициялық өзгерістерден және кванттық шектелуден бірнеше механизмдер арқылы болуы мүмкін.[16] Бұған LaAlO мысалы бола алады3 SrTiO өсірілген3, қайда интерфейс өткізгіштікті көрсете алады, тіпті LaAlO болса да3 және SrTiO3 өткізгіш емес.[17]
Мысалдар
Минералдар
Перовскит құрылымы жоғары қысымда қабылданады бридгманит, формуласы бар силикат (Mg, Fe) SiO3, бұл мантиядағы ең көп таралған минерал. Қысым жоғарылаған сайын SiO44− құрамында кремнийі бар минералдардағы тетраэдрлік қондырғылар SiO-мен салыстырғанда тұрақсыз болады68− сегіздік бірліктер. Төменгі мантияның қысымы мен температуралық жағдайында, ең көп екінші материал болуы мүмкін құрылымдар (Mg, Fe) O оксиді, периклаз.[2]
Жердің жоғары қысым жағдайында төменгі мантия, пироксен энстатит, MgSiO3, тығыз перовскит құрылымды түрге айналады полиморф; бұл фаза Жердегі ең көп таралған минерал болуы мүмкін.[18] Бұл фаза орторомбалық бұрмаланған перовскиттік құрылымға ие (GdFeO)3~ типі құрылымы) ~ 24 ГПа-дан ~ 110 ГПа-ға дейінгі қысым кезінде тұрақты. Алайда, оны бірнеше жүз км тереңдіктен Жер бетіне дейін аз тығыз материалдарға айналдырмай тасымалдау мүмкін емес. Жоғары қысым кезінде, MgSiO3 перовскит, әдетте силикат перовскиті ретінде белгілі, айналады кейінгі перовскит.
Басқалар
Перовскиттің кең таралған қосылыстарында оттегі болғанымен, оттексіз түзілетін бірнеше перовскиттік қосылыстар бар. NaMgF сияқты фторлы перовскиттер3 белгілі. Металл перовскит қосылыстарының үлкен тобын RT ұсынуы мүмкін3M (R: сирек жер немесе басқа салыстырмалы түрде үлкен ион, Т: ауыспалы метал ионы және M: жеңіл металлоидтар). Металлоидтар осы қосылыстардағы октаэдралық үйлестірілген «В» учаскелерін алады. RPd3B, RRh3B және CeRu3C - мысалдар. MgCNi3 металл перовскит қосылысы болып табылады және оның өткізгіштік қасиетіне байланысты көп көңіл бөлінді. Перовскиттің одан да экзотикалық түрі Cs және Rb аралас оксид-ауридтерімен ұсынылған, мысалы Cs3Дәстүрлі «анион» алаңдарында үлкен сілтілі катиондар бар AuO, О-мен байланысқан2− және Au− аниондар.[дәйексөз қажет ]
Материалдардың қасиеттері
Перовскит материалдары теориялық жағынан да, қолдану тұрғысынан да көптеген қызықты және қызықты қасиеттерді көрсетеді. Үлкен магниттік кедергі, электр қуаты, асқын өткізгіштік, ақыға тапсырыс беру, спинге тәуелді тасымалдау, жоғары жылу қуаты және құрылымдық, магниттік және транспорттық қасиеттердің өзара әрекеттесуі осы отбасында байқалады. Бұл қосылыстар датчиктер және катализатор электродтары ретінде белгілі бір түрлерінде қолданылады отын элементтері[19] және жад құрылғыларына үміткерлер болып табылады және спинтроника қосымшалар.[20]
Көптеген асқын өткізгіштік қыш материалдар ( жоғары температуралы асқын өткізгіштер ) құрамында перовскит тәрізді құрылымдар бар, көбінесе 3 немесе одан да көп металды мыспен қоса, кейбір оттегі позициялары бос қалады. Бір жақсы мысал иттрий барий мыс оксиді оттегінің құрамына байланысты оқшаулағыш немесе асқын өткізгіш болуы мүмкін.
Химия инженерлері кобальт негізіндегі перовскит материалын in платинаны алмастыру ретінде қарастырады каталитикалық түрлендіргіштер дизельді көліктерге арналған.[21]
Қолданбалар
Қызығушылықтың физикалық қасиеттері материалтану перовскиттерге жатады асқын өткізгіштік, магниттік кедергі, иондық өткізгіштік, және микроэлектроникада үлкен маңызы бар диэлектрлік қасиеттердің көптігі және телекоммуникация. Олар сондай-ақ кейбір мүдделер үшін сцинтиллятор өйткені олар радиациялық түрлендіру үшін үлкен жарық береді. Перовскит құрылымына тән байланыс бұрыштарының икемділігі арқасында идеал құрылымнан болатын әр түрлі бұрмаланулар бар. Оларға қисаю жатады октаэдра, координаттардың координация центрлерінен катиондардың ығысуы және октаэдраның бұрмалануы электронды факторлар (Джен-Теллердің бұрмалаулары ).[22]
Фотоэлектриктер

Синтетикалық перовскиттер тиімділігі жоғары коммерциялық арзан материалдар ретінде анықталды фотоэлектрлік[24][25] - олар NREL 2020 жылы есеп берген 25,5% дейін конверсия тиімділігін көрсетті[25][26][27] және жұқа қабатты кремнийлі күн батареялары үшін қолданылатын жұқа қабықшаларды жасау тәсілдерін қолдану арқылы өндіруге болады.[28] Метиламмоний қалайы галогенидтері және метиламмоний қорғасын галогенидтері пайдалану үшін қызығушылық тудырады бояуға сезімтал күн батареялары.[29][30] 2016 жылдың шілдесінде доктор Александр Вебер-Баргиони бастаған зерттеушілер тобы перовскиттің ПВ жасушаларының теориялық шыңына 31% жететіндігін көрсетті.[31]
Осы уақытқа дейін зерттелген метиламмоний галогенидтерінің ішінде метиламмоний қорғасын триоидиді (CH
3NH
3PbI
3). Бұл жоғары заряд тасымалдаушы жарық пен электрондар мен саңылаулар жасуша ішіндегі жылу ретінде энергиясын жоғалтпаудың орнына, оларды ток ретінде алуға болатындай алысқа жылжуға мүмкіндік беретін қозғалғыштық және заряд тасымалдаушының қызмет ету мерзімі. CH
3NH
3PbI
3 тиімді диффузиялық ұзындықтар электрондар үшін де, тесіктер үшін де 100 нм құрайды.[32]
Метиламмоний галогенидтері төмен температуралы ерітінді әдістерімен тұндырылады (әдетте айналдыру ). Ерітіндімен өңделген басқа төмен температуралы (100 ° C-тан төмен) қабықшалардың диффузия ұзындығы едәуір аз болады. Стрэнкс және басқалар. сипатталған наноқұрылымды аралас метиламмоний қорғасын галогенін қолданатын жасушалар (CH3NH3PbI3 − xClх) және 11,4% конверсия тиімділігі бар бір аморфты жұқа қабықшалы күн батареясын көрсетті, ал басқасын пайдаланып 15,4% -ға жетті. вакуумдық булану. Қабыршақтың қалыңдығы шамамен 500-ден 600 нм-ге дейін, электрондар мен саңылаулардың диффузия ұзындығы осы тәртіптен кем болмайтындығын білдіреді. Олар диффузияның ұзындығының мәндерін таза иодид үшін 100 нм-ден жоғары реті бар аралас перовскит үшін 1 мкм-ден жоғары өлшеді. Сонымен қатар олар аралас перовскиттегі тасымалдаушының өмір сүру уақыты таза йодидке қарағанда ұзағырақ екенін көрсетті.[32] Лю және т.б. (110) жазықтық бойымен аралас галогенді перовскиттегі электрондардың диффузиялық ұзындығы 10 мкм болатындығын көрсету үшін фотокөшіру сканерлеу қолданылды.[33]
Үшін CH
3NH
3PbI
3, ашық тізбектегі кернеу (VOC) әдетте 1 В-қа жақындайды, ал үшін CH
3NH
3PbI (I, Cl)
3 құрамында Cl мөлшері аз, VOC > 1.1 В хабарланды. Себебі жолақ аралықтары (Eж) екеуі де 1,55 эВ, VOC- Е.ж коэффициенттері ұқсас үшінші ұрпақ жасушаларында байқалатыннан гөрі жоғары. Кеңірек перовскиттермен В.OC 1,3 В дейін көрсетілген.[32]
Техника төмен температуралық әлеуетті ұсынады, себебі төмен температуралық ерітінді әдістері және сирек кездесетін элементтер жоқ. Қазіргі уақытта жасушалардың беріктігі коммерциялық мақсатта пайдалану үшін жеткіліксіз.[32]
Персовскитті күн батареяларының жазықтықтағы гетеродукциясы тек будың тұндырылуын қолдана отырып, құрылғының қарапайым құрылымында (күрделі наноқұрылымсыз) жасалуы мүмкін. Бұл әдіс күн сәулесінен электр қуатын 15% түрлендіруге мүмкіндік береді, ол күн сәулесінің толық сәулеленуі кезінде өлшенеді.[34]
Лазерлер
2008 жылы зерттеушілер перовскиттің генерациялай алатынын көрсетті лазер жарық. LaAlO3 қосылды неодим лазерлік сәуле шығаруды 1080 нм-де берді.[35] 2014 жылы метиламмоний қорғасын галогенидінің (CH3NH3PbI3 − xClх) оптикалық айдалатын тік қуысты лазерлерге (VCSEL) сәйкес жасушалар көрінетін сорғы жарығын 70% тиімділікпен ИҚ-ға жақын лазер сәулесіне айналдырады.[36][37]
Жарық диодтары
Жоғары фотолюминесценциясының арқасында кванттық тиімділік, перовскиттер қолдануға жақсы үміткерлер болуы мүмкін жарық диодтары (Жарық диоды).[38] Алайда, бейімділік радиациялық рекомбинация көбінесе сұйық азот температурасында байқалды.
Фотоэлектролиз
2014 жылдың қыркүйегінде Швейцарияның Лозанна қаласындағы EPFL зерттеушілері суды электролизге 12,3% тиімділікпен перовскиттік фотоэлектриктерді қолданып, өте тиімді және арзан су бөлетін жасушада қол жеткізді деп хабарлады.[39][40]
Сцинтилляторлар
1997 жылы церий қоспасы бар лютеций алюминий перовскитінің (LuAP: Ce) бір кристалдарының сцинтилляциялық қасиеттері туралы хабарлады.[41] Сол кристалдардың басты қасиеті - массаның тығыздығы 8,4 г / см3, бұл қысқа рентгендік және гамма-сәулелік сіңіру ұзындығын береді. Сцинтилляцияның жарық түсімі және C-мен ыдырау уақыты137 сәулелену көзі сәйкесінше 11 400 фотон / МэВ және 17 нс құрайды. Бұл қасиеттер LUAP: Ce сцинтилляторларын жарнамалық роликтер үшін тартымды етті және олар жоғары энергетикалық физикада жиі қолданылды. Он бір жылға дейін Жапониядағы бір топ Радлсден-Поппер ерітіндісіне негізделген гибридті органикалық-органикалық емес перовскит кристалдарын арзан сцинтиллятор ретінде ұсынды.[42] Алайда, қасиеттері LuAP: Ce-мен салыстырғанда онша әсерлі болған жоқ. Келесі тоғыз жылға дейін ерітіндіге негізделген гибридті органикалық-органикалық емес перовскит кристалдары олардың криогендік температурада 100000 фотон / МэВ-тан жоғары жарық өнімділігі туралы есеп беру арқылы қайта танымал болды.[43] Соңында, рентгендік бейнелеу экранына арналған перовскиттік нанокристалды сцинтилляторлардың керемет демонстрациясы туралы айтылды және бұл перовскиттік сцинтилляторлар үшін көбірек зерттеу жұмыстарын бастады.[44]
Перовскиттердің мысалдары
Қарапайым:
- Стронций титанаты
- Кальций титанаты
- Қорғасын титанат
- Висмут ферриті
- Лантан итербий оксиді
- Силикатты перовскит
- Лантан марганиті
- Итрий алюминий перовскиті (ЯП)
- Лютеций алюминий перовскиті (LuAP)
- Лантан стронций марганиті
- LSAT (лантан алюминаты - стронций алюминий танталаты)
- Қорғасын скандийі танталаты
- Қорғасын цирконаты титанаты
- Метиламмоний қорғасын галогенид
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ А.Навроцкий (1998). «Ильменит, литий ниобаты және перовскит құрылымдары арасындағы энергетика және кристалды химиялық жүйелеу». Хим. Mater. 10 (10): 2787. дои:10.1021 / cm9801901.
- ^ а б c Венк, Ханс-Рудольф; Булах, Андрей (2004). Пайдалы қазбалар: олардың конституциясы және шығу тегі. Нью-Йорк, Нью-Йорк: Кембридж университетінің баспасы. ISBN 978-0-521-52958-7.
- ^ Артини, Кристина (2017-02-01). «Кристалдық химия, тұрақтылық және интертанидті перовскиттердің қасиеттері: шолу». Еуропалық керамикалық қоғам журналы. 37 (2): 427–440. дои:10.1016 / j.jeurceramsoc.2016.08.041. ISSN 0955-2219.
- ^ Бриджеманит қосулы Mindat.org
- ^ Фан, Чжен; Күн, Қуан; Ванг, Джон (2015-09-15). «Фотоэлектрлік перовскиттер: органикалық-бейорганикалық галогенді перовскиттер мен ферроэлектрлік оксидті перовскиттердің жиынтық шолуы». Материалдар химиясы журналы А. 3 (37): 18809–18828. дои:10.1039 / C5TA04235F. ISSN 2050-7496.
- ^ Джонсон, Матс; Лемменс, Питер (2007). «Перовскиттердің кристаллографиясы және химиясы». Магнетизм және жетілдірілген магниттік материалдар туралы анықтама. arXiv:cond-mat / 0506606. дои:10.1002 / 9780470022184.hmm411. ISBN 978-0470022177. S2CID 96807089.
- ^ Кава, Роберт Дж. «Кава зертханасы: перовскиттер». Принстон университеті. Алынған 13 қараша 2013.
- ^ Кендалл, К.Р .; Навас, С .; Томас, Дж. К .; Зур Лойе, H. C. (1996). «Оксид-ион өткізгіштерінің соңғы дамуы: Оривиллий фазалары». Материалдар химиясы. 8 (3): 642–649. дои:10.1021 / cm9503083.
- ^ а б Муннингс, С; Скиннер, С; Аму, Г; Уитфилд, П; Дэвидсон, I (15 қазан 2006). «Ла құрылымы, тұрақтылығы және электрлік қасиеттері(2 − x)SrхMnO4 ± δ қатты ерітінді сериясы «. Қатты күйдегі ионика. 177 (19–25): 1849–1853. дои:10.1016 / j.ssi.2006.01.009.
- ^ Мэннингс, Кристофер Н .; Сайерс, Рут; Стюарт, Пол А .; Скиннер, Стивен Дж. (Қаңтар 2012). «Sr құрылымдық трансформациясы және тотығуы2MnO3,5 + x орнында нейтронды ұнтақ дифракциясы арқылы анықталады « (PDF). Қатты дене ғылымдары. 14 (1): 48–53. Бибкод:2012SSSci..14 ... 48M. дои:10.1016 / j.solidstatescience.2011.10.015. hdl:10044/1/15437.
- ^ Амов, Г .; Уитфилд, П. С .; Дэвидсон, Дж .; Хаммонд, Р.П .; Муннингс, C. Н .; Skinner, S. J. (қаңтар 2004). «Ла құрылымдық және агломерациялық сипаттамалары2Ни1 − xCoхO4 + δ серия «. Халықаралық керамика. 30 (7): 1635–1639. дои:10.1016 / j.ceramint.2003.12.164.
- ^ Амов, Г .; Уитфилд, П. С .; Дэвидсон, Дж .; Хаммонд, Р.П .; Мэннингс, С .; Скиннер, С. (11 ақпан 2011). «Гиперстоихиометриялық серияның құрылымдық және физикалық меншік тенденциялары, La2Ни(1−х)CoхO4 + δ". MRS іс жүргізу. 755. дои:10.1557 / PROC-755-DD8.10.
- ^ Мартин, Л.В .; Чу, Ю.-Х .; Рамеш, Р. (мамыр 2010). «Магнитті, ферроэлектрлік және мультиферротық оксидті жұқа қабықшалардың өсуі мен сипаттамасындағы жетістіктер». Материалтану және инженерия: R: Есептер. 68 (4–6): 89–133. дои:10.1016 / j.mser.2010.03.001.
- ^ Янг, Г.З; Лу, Н.Б; Чен, Ф; Чжао, Т; Chen, ZH (шілде 2001). «Лазерлі молекулалық сәуленің эпитаксиясы және перовскит оксидінің жұқа қабықшаларының сипаттамасы». Хрусталь өсу журналы. 227-228: 929–935. дои:10.1016 / S0022-0248 (01) 00930-7.
- ^ Манхарт, Дж .; Schlom, D. G. (25 наурыз 2010). «Оксидтік интерфейстер - электроникаға арналған мүмкіндік». Ғылым. 327 (5973): 1607–1611. дои:10.1126 / ғылым.1181862. PMID 20339065. S2CID 206523419.
- ^ Чахалян Дж .; Миллис, А. Дж .; Rondinelli, J. (24 қаңтар 2012). «Қай жерде оксид интерфейсі». Табиғи материалдар. 11 (2): 92–94. дои:10.1038 / nmat3225. PMID 22270815.
- ^ Охтомо, А .; Hwang, H. Y. (қаңтар 2004). «LaAlO3 / SrTiO3 гетероинтерфейсіндегі жоғары қозғалмалы электронды газ». Табиғат. 427 (6973): 423–426. дои:10.1038 / табиғат02308. PMID 14749825. S2CID 4419873.
- ^ Джон Ллойд; Джон Митчинсон (2006). «Әлемдегі ең көп таралған материал». QI: Жалпы надандық туралы кітап. Faber & Faber. ISBN 978-0-571-23368-7.
- ^ Кулкарни, А; Циакчи ФТ; С Гидди; С Муннингс; т.б. (2012). «Аралас ионды электронды өткізгіш перовскитті анод, тікелей көміртекті отын элементтері үшін». Сутегі энергиясының халықаралық журналы. 37 (24): 19092–19102. дои:10.1016 / j.ijhydene.2012.09.141.
- ^ Дж. Д. Д. Кой; М. Вирет; С. фон Молнар (1999). «Аралас валентті манганиттер». Физикадағы жетістіктер. 48 (2): 167–293. Бибкод:1999AdPhy..48..167C. дои:10.1080/000187399243455.
- ^ Александра Витзе (2010). «Арзан катализатор құру». Science News веб-басылымы.
- ^ Люфасо, Майкл В. Вудворд, Патрик М. (2004). «Перовскиттердегі кахиондардың бұрмалануы, катиондарға тапсырыс беру және октаэдрлік қисаю». Acta Crystallographica бөлімі B. 60 (Pt 1): 10-20. дои:10.1107 / S0108768103026661. PMID 14734840.
- ^ Эймес, Кристофер; Аяз, Ярвист М .; Барнс, Пирс Р.Ф .; Реган, Брайан С .; Уолш, Арон; Ислам, М.Сайфул (2015). «Иодты тасымалдау гибридті қорғасын иодидті перовскитті күн батареяларында». Табиғат байланысы. 6: 7497. Бибкод:2015NatCo ... 6.7497E. дои:10.1038 / ncomms8497. PMC 4491179. PMID 26105623.
- ^ Буллис, Кевин (8 тамыз 2013). «Күн қуатын тудыратын материал» лас арзан"". MIT Technology шолуы. Алынған 8 тамыз 2013.
- ^ а б Ли, Ханцян. (2016). «Перовскитті күн батареяларын жасау үшін модификацияланған дәйекті тұндыру әдісі». Күн энергиясы. 126: 243–251. Бибкод:2016SoEn..126..243L. дои:10.1016 / j.solener.2015.12.045.
- ^ «Зерттеу жасушаларының тиімділігі туралы жазбалар» (PDF). Энергия тиімділігі және жаңартылатын энергия бөлімі. 2020.
- ^ Чжу, Руй (2020-02-10). «Төңкерілген құрылғылар қуып жетуде». Табиғат энергиясы. 5 (2): 123–124. дои:10.1038 / s41560-020-0559-z. ISSN 2058-7546. S2CID 213535738.
- ^ Лю, Минчжэнь; Джонстон, Майкл Б .; Снайт, Генри Дж. (2013). «Перовскитті күн батареяларын булардың тұндыруымен тиімді жазықтықтағы гетерожанкция». Табиғат. 501 (7467): 395–398. Бибкод:2013 ж.т.501..395L. дои:10.1038 / табиғат 12509. PMID 24025775. S2CID 205235359.
- ^ Lotsch, BV (2014). «Ескі оқиғаға жаңа нұр: перовскиттер күн сәулесіне түседі». Angew. Хим. Int. Ред. 53 (3): 635–637. дои:10.1002 / anie.201309368. PMID 24353055.
- ^ Service, R. (2013). «Жарықты қосу». Ғылым. 342 (6160): 794–797. дои:10.1126 / ғылым.342.6160.794. PMID 24233703.
- ^ «Наноөлшемді жаңалық перовскитті күн батареяларын 31% тиімділікке жеткізуі мүмкін». 2016-07-04.
- ^ а б c г. Hodes, G. (2013). «Перовскит негізіндегі күн ұяшықтары». Ғылым. 342 (6156): 317–318. Бибкод:2013Sci ... 342..317H. дои:10.1126 / ғылым.1245473. PMID 24136955. S2CID 41656229.
- ^ Лю, Шухао; Ванг, Лили; Лин, Вэй-Чун; Сучаритакул, Сукрит; Бурда, Клеменс; Гао, Xuan P. A. (2016-12-14). «Бағдарланған перовскиттік фильмдерде фототасымалдағыштардың ұзақ тасымалдау ұзындығын кескіндеу». Нано хаттары. 16 (12): 7925–7929. arXiv:1610.06165. Бибкод:2016NanoL..16.7925L. дои:10.1021 / acs.nanolett.6b04235. ISSN 1530-6984. PMID 27960525. S2CID 1695198.
- ^ Лю М .; Джонстон, М.Б .; Snaith, H. J. (2013). «Перовскитті күн батареяларын булардың тұндыруымен тиімді жазықтықтағы гетерожанкция». Табиғат. 501 (7467): 395–398. Бибкод:2013 ж.т.501..395L. дои:10.1038 / табиғат 12509. PMID 24025775. S2CID 205235359.
- ^ Dereń, P. J .; Беднаркевич, А .; Голднер, Ph .; Guillot-Noël, O. (2008). «LaAlO-дағы лазерлік әрекет3: Nd3+ жалғыз кристалл ». Қолданбалы физика журналы. 103 (4): 043102–043102–8. Бибкод:2008ЖАП ... 103d3102D. дои:10.1063/1.2842399.
- ^ Уоллес, Джон (28 наурыз 2014) Перовскиттің жоғары тиімділігі бар фотоэлектрлік материал да лазирлейді. LaserFocusWorld
- ^ «Зерттеу: Перовскит күн батареялары лазерге қосыла алады». Rdmag.com. 2014-03-28. Алынған 2014-08-24.
- ^ Стрэнкс, Сэмюэл Д .; Снайт, Генри Дж. (2015-05-01). «Фотоэлектрлік және жарық шығаратын құрылғыларға арналған металл-галогенді перовскиттер». Табиғат нанотехнологиялары. 10 (5): 391–402. Бибкод:2015NatNa..10..391S. дои:10.1038 / nnano.2015.90. ISSN 1748-3387. PMID 25947963.
- ^ Джингшан Луо; т.б. (26 қыркүйек 2014). «Перовскитті фотоэлектриктер және жердегі катализаторлар арқылы 12,3% тиімділікпен суды фотолиздеу». Ғылым. 345 (6204): 1593–1596. Бибкод:2014Sci ... 345.1593L. дои:10.1126 / ғылым.1258307. PMID 25258076. S2CID 24613846.
- ^ «Жерден мол материалдарды пайдаланып, Күннен сутегі отынын жинау». Phys.org. 25 қыркүйек 2014 ж. Алынған 26 қыркүйек 2014.
- ^ Мозынский, М (11 қаңтар 1997). «Жаңа LuAP қасиеттері: Ce сцинтилляторы». Ядролық инст. Ал физиканы зерттеу әдістері А. 385: 123–131. дои:10.1016 / S0168-9002 (96) 00875-3.
- ^ Кишимото, С (29 желтоқсан 2008). «Органикалық-бейорганикалық перовскиттік сцинтилляторды қолдану арқылы субнаносекундтық рентгендік өлшеулер». Қолдану. Физ. Летт. 93 (26): 261901. Бибкод:2008ApPhL..93z1901K. дои:10.1063/1.3059562.
- ^ Бировосуто, Мухаммад Дананг (16 қараша 2016). «Қорғасын галоидті перовскит кристалдарындағы рентгендік сцинтилляция». Ғылыми. Rep. 6: 37254. arXiv:1611.05862. Бибкод:2016 жыл НАТСР ... 637254B. дои:10.1038 / srep37254. PMC 5111063. PMID 27849019.
- ^ Чен, Куишуи (27 тамыз 2018). «Барлық бейорганикалық перовскиттік нанокристалды сцинтилляторлар». Табиғат. 561 (7721): 88–93. дои:10.1038 / s41586-018-0451-1. PMID 30150772. S2CID 52096794.
Әрі қарай оқу
- Теджука, Луис Г (1993). Перовскит типіндегі оксидтердің қасиеттері мен қолданылуы. Нью-Йорк: Деккер. б. 382. ISBN 978-0-8247-8786-8.
- Митчелл, Роджер Н (2002). Перовскиттер қазіргі және ежелгі. Thunder Bay, Онтарио: Алмаз Пресс. б. 318. ISBN 978-0-9689411-0-2.
Сыртқы сілтемелер
- «Кубтық перовскит құрылымы». Материалдарды есептеу орталығы. АҚШ әскери-теңіз зертханасы. Архивтелген түпнұсқа 2008-10-08. (а кіреді Java апплеті құрылымды интерактивті түрде айналдыруға болады)
