Қалайы (II) фтор - Tin(II) fluoride
 Sn2+; F− | |
| Атаулар | |
|---|---|
| IUPAC атауы Қалайы (II) фтор | |
| Басқа атаулар Тұрақты фтор | |
| Идентификаторлар | |
3D моделі (JSmol ) | |
| ECHA ақпарат картасы | 100.029.090 |
PubChem CID | |
| RTECS нөмірі |
|
| UNII | |
| БҰҰ нөмірі | 3288 |
CompTox бақылау тақтасы (EPA) | |
| |
| |
| Қасиеттері | |
| SnF2 | |
| Молярлық масса | 156,69 г / моль |
| Сыртқы түрі | түссіз қатты |
| Тығыздығы | 4,57 г / см3 |
| Еру нүктесі | 213 ° C (415 ° F; 486 K) |
| Қайнау температурасы | 850 ° C (1,560 ° F; 1,120 K) |
| 31 г / 100 мл (0 ° C); 35 г / 100 мл (20 ° C); 78,5 г.100 мл (106 ° C) | |
| Ерігіштік | ериді KOH, KF; жылы этанол, эфир, хлороформ |
| Құрылым | |
| Моноклиника, mS48 | |
| C2 / c, №15 | |
| Фармакология | |
| A01AA04 (ДДСҰ) | |
| Қауіпті жағдайлар | |
| Қауіпсіздік туралы ақпарат парағы | ICSC 0860 |
| NFPA 704 (от алмас) | |
| Тұтану температурасы | Жанғыш емес |
| Байланысты қосылыстар | |
Басқа аниондар | Қалайы (II) хлорид, Қалайы (II) бромид, Қалайы (II) йодид |
Басқа катиондар | Германий тетрафторид, Қалайы тетрафторид, Қорғасын (II) фтор |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
Қалайы (II) фтор, әдетте коммерциялық деп аталады тұрақты фтор[1][2] (бастап.) Латын stannum, 'қалайы'), а химиялық қосылыс SnF формуласымен2. Бұл ингредиент ретінде қолданылатын түссіз қатты зат тіс пасталары.
Қуыстың алдын алу
Флоридке балама ретінде енгізілді натрий фторы қуыстардың алдын алу үшін. Оны Джозеф Мухлер мен Уильям Небергалл осы мақсатта енгізген. Жаңашылдықтары үшін бұл екі адам Өнертапқыштар Даңқ залына енгізілді.[1]
Стандартты фтор кальций минералын айналдырады апатит ішіне фторапатит жасайды тіс эмаль бактериялар тудыратын төзімді қышқыл шабуылдар.[3] Тіс пасталарының көпшілігінде кальций минералдары бар[дәйексөз қажет ]; уақыт өте келе олар натрий фторидімен әрекеттесіп түзіледі фторлы кальций, бұл толығымен ерімейді, сондықтан тісті қорғау үшін тиімсіз. Тұрақты фтор - бұл тұрақты ингредиент, сондықтан ұзақ сақтаған кезде тіс эмальын күшейтеді.[4] Станоктық фтор сияқты тиімді екені дәлелденді натрий фторы стоматологиялық кариес ауруының төмендеуінде[5] және бақылау гингивит.[6]
Астында фтанид қолданылды Сауда атауы Флуористан тіс пастасы брендінің түпнұсқа құрамындағы Crest, кейінірек ол ауыстырылды натрий монофторофосфаты Fluoristat сауда атауымен. Тұрақты фтор - Crest Pro Health брендінің тіс пастасының белсенді ингредиенті. Crest Pro Health түтікке фтордың бояуы мүмкін екенін ескертеді, оны дұрыс щеткамен аулақ болуға болады және оның белгілі бір формуласы бояуға төзімді. Алайда, дұрыс емес щеткамен пайда болатын кез-келген фторлы стендтер тұрақты болмайды. Станоктық фтор сонымен қатар қолданылады Oral-B Pro-Expert.[7] Фторлы флорид рецептсіз шаю кезінде де қол жетімді.
Өндіріс
SnF2 SnO ерітіндісін 40% буландыру арқылы дайындауға болады HF.[8]
- SnO + 2 HF → SnF2 + H2O
Сулы ерітінділер
Суда оңай ериді, SnF2 гидролизденеді. Төмен концентрацияда ол SnOH сияқты түрлер құрайды+, Sn (OH)2 және Sn (OH)3−. Жоғары концентрацияда көбінесе полинуклеарлы түрлер, соның ішінде Sn түзіледі2(OH)22+ және Sn3(OH)42+.[9] Су ерітінділері тез тотығып, Sn-дің ерімейтін тұнбаларын түзедіIV, олар стоматологиялық профилактика ретінде тиімсіз.[10] Тотығуды қолдану арқылы зерттеу Мессбауэр спектроскопиясы мұздатылған үлгілерде О2 тотықтырғыш түрі болып табылады.[11]
Льюис қышқылдығы
SnF2 ретінде әрекет етеді Льюис қышқылы. Мысалы, ол 1: 1 кешенін құрайды (CH3)3NSnF2 және 2: 1 кешен [(CH3)3N]2SnF2 бірге триметиламин,[12] және 1: 1 кешені бар диметилсульфоксид, (CH3)2SO · SnF2.[13]
Фтор ионы бар ерітінділерде Ф−, бұл SnF фторлы кешендерін құрайды3−, Sn2F5−және SnF2(OH2).[14] Құрамындағы сулы ерітіндіден кристалдану NaF құрамында полинуклеарлы аниондар бар қосылыстар шығарады, мысалы. NaSn2F5 немесе Na4Sn3F10 NaSnF емес, реакция жағдайына байланысты3.[8] NaSnF қосылысы3құрамында пирамидалы SnF бар3− анионды пиридин-су ерітіндісінен алуға болады.[15] Құрамында пирамидалы SnF бар басқа қосылыстар3− анионы белгілі, мысалы Ca (SnF)3)2.[16]
Қасиеттерін төмендету
SnF2 Бұл редуктор, E стандартты төмендету потенциалыменo (SnIV/ SnII) = +0,15 В.[17] HF-дегі ерітінділер тотықтырғыш заттардың (O.) Диапазонымен оңай тотығады2, SO2 немесе F2) аралас валентті қосылыс Sn түзеді3F8 (құрамында SnII және SnIV және Sn-Sn байланысы жоқ).[8]
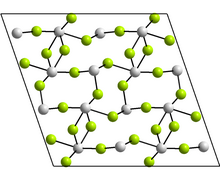
Құрылым
Моноклиникалық формада тетрамерлер, Sn4F8, онда Sn атомдары үшін екі нақты үйлестіру ортасы бар. Екі жағдайда да үш жақын көршіміз бар, олардың үшеуі тригональды пирамида шыңында, ал жалғыз жұп электрондар стерикалық белсенді.[18] Басқа нысандарда бар GeF2 және парателлурит құрылымдар.[18]
Молекулалық SnF2
Бу фазасында SnF2 мономерлер, димерлер және тримерлер құрайды.[14] Monomeric SnF2 - бұл сызықты емес молекула, Sn Sn-F байланысының ұзындығы 206 pm.[14] SnF кешендері2, кейде дифлюростаннилен деп аталады, алкон мен ароматты қосылыстардың аргон матрицасына 12 К-ге түскені туралы айтылған.[19][20]
Қауіпсіздік
Тұрақты фтор, егер ол деммен жұтылса немесе көзге түссе, қызару мен тітіркенуді тудыруы мүмкін. Жедел деңгейде (2 мг / м-ден жоғары)3), егер ішке қабылданса, іштің ауыруы және шок болуы мүмкін.[21] Сирек, бірақ ауыр аллергиялық реакциялар мүмкін; белгілеріне қышу, ісіну және тыныс алудың қиындауы жатады. Стоматологиялық өнімдерде қолданылған кезде, жұмсақ тістің түсінің өзгеруі болуы мүмкін; оны щеткамен жоюға болады.[22]
Әдебиеттер тізімі
- ^ а б «Ұлттық өнертапқыштар даңқы залы CES-те 2019 индукцияланған адамдар туралы жариялады». Ұлттық өнертапқыштар даңқы залы. Алынған 6 ақпан 2019.
- ^ «Латынша атаулары айнымалы зарядталатын металдар». Nobel.SCAS.BCIT.ca/. Британдық Колумбия технологиялық институты химия бөлімі. Алынған 16 маусым 2013.
- ^ Гроэневельд, А .; Пурделл-Льюис, Дж .; Арендс, Дж. (1976). «Жасанды кариестің зақымдануын флоридпен реминерализациялау». Кариесті зерттеу. 10 (3): 189–200. дои:10.1159/000260201. ISSN 0008-6568. PMID 1063601.
- ^ Хаттаб, Ф. (сәуір, 1989). «Фторидтердің тіс пасталарындағы күйі». Стоматология журналы. 17 (2): 47–54. дои:10.1016/0300-5712(89)90129-2. PMID 2732364.
- ^ Невитт Г.А., Witter DH, Bowman WD (қыркүйек 1958). «Фторлы натрий мен флоридтің жергілікті қолданылуы». Қоғамдық денсаулық сақтау. 73 (9): 847–50. дои:10.2307/4590256. JSTOR 4590256. PMC 1951625. PMID 13579125.
- ^ Перлич, MA; Бакка, Лос-Анджелес; Боллмер, BW; Ланзалако, айнымалы ток; Маккланахан, СФ; Севак, ЛК; Бейсвангер, Б.Б; Эйхольд, АҚШ; т.б. (1995). «Флоридті тұрақтандырылған тұрақтандырғыш фланецтің бляшек түзілуіне, гингивитке және тіс қанынан қан кетуіне клиникалық әсері: алты айлық зерттеу». Клиникалық стоматология журналы. 6 (Арнайы шығарылым): 54–58. PMID 8593194.
- ^ Lippert F, Newby EE, Lynch RJ, Chauhan VK, Schemehorn BR (2009). «Жаңа тіс емдеу құралының антикариялық әлеуетін зертханалық бағалау». J Clin Dent. 20 (2): 45–9. PMID 19591336.
- ^ а б c Гринвуд, Норман Н.; Эрншоу, Алан (1997). Элементтер химиясы (2-ші басылым). Баттеруорт-Хейнеманн. ISBN 978-0-08-037941-8.
- ^ Себи Ф., Потин-Готье М., Гиффо Э., Донард О. Ф. Х .; Потин-Готье; Гиффо; Донард (2001). «Бейорганикалық қалайының түрлеріне арналған термодинамикалық деректерге сыни шолу». Geochimica et Cosmochimica Acta. 65 (18): 3041–3053. Бибкод:2001GeCoA..65.3041S. дои:10.1016 / S0016-7037 (01) 00645-7.CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ Дэвид Б. Трой, 2005, Ремингтон: Фармация ғылымы мен практикасы, Липпинкотт Уильямс және Уилкинс, ISBN 0-7817-4673-6, ISBN 978-0-7817-4673-1
- ^ Denes G; Лазанас Г .; Лазанас (1994). «SnF тотығуы2 судағы ерітінділердегі тұрақты фтор ». Гиперфинмен өзара әрекеттесу. 90 (1): 435–439. Бибкод:1994HyInt..90..435D. дои:10.1007 / BF02069152. S2CID 96184099.CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ Чун Чун Хсу және Р.А. Геангел (1977). «Триметиламиннің қосылыстарын қалайы (II) галогенидтерімен синтездеу және зерттеу». Инорг. Хим. 16 (1): 2529–2534. дои:10.1021 / ic50176a022.
- ^ Чун Чун Хсу және Р.А. Геангел (1980). «Екі валентті қалайы қосылыстарының донорлық және акцепторлық әрекеті». Инорг. Хим. 19 (1): 110–119. дои:10.1021 / ic50203a024.
- ^ а б c Эгон Уайберг, Арнольд Фредерик Холлеман (2001) Бейорганикалық химия, Elsevier ISBN 0-12-352651-5.
- ^ Salami T. O., Zavalij P. Y. және Oliver S.R J. (2004). «Фторлы қалайының екі қалайының синтезі және кристалдық құрылымы: NaSnF3 (BING-12) және Sn3F3PO4". Қатты күйдегі химия журналы. 177 (3): 800–805. Бибкод:2004JSSCh.177..800S. дои:10.1016 / j.jssc.2003.09.013.
- ^ Кокунов Ю.В .; Детков Д.Г .; Горбунова Ю. Е .; Ершова М.М .; Михайлов Ю. N. (2001). «Кальций трифторостаннатының синтезі және кристалдық құрылымы (II)». Doklady Химиясы. 376 (4–6): 52–54. дои:10.1023 / A: 1018855109716. S2CID 91430538.
- ^ Housecroft, C. E .; Шарп, А.Г. (2004). Бейорганикалық химия (2-ші басылым). Prentice Hall. ISBN 978-0-13-039913-7.
- ^ а б Уэллс А.Ф. (1984) Құрылымдық бейорганикалық химия 5-ші шығарылым Oxford Science Publications ISBN 0-19-855370-6
- ^ С. Е.Боганов, В. И. Фаустов, М. П. Егоров және О. М. Нефедов (1994). «Матрицалық ИҚ-спектрлері және дифлуортаннилен мен гепт-1-йен арасындағы реакцияны кванттық химиялық зерттеу. Карбин аналогы π-кешенін алкинмен алғашқы тікелей бақылау». Ресейлік химиялық бюллетень. 43 (1): 47–49. дои:10.1007 / BF00699133. S2CID 97064510.CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме)
- ^ С. Е.Боганов, М. П. Егоров және О. М. Нефедов (1999). «Дифлюростаннилен мен хош иісті заттар арасындағы комплексті ИК-спектроскопия матрицасы арқылы зерттеу». Ресейлік химиялық бюллетень. 48 (1): 98–103. дои:10.1007 / BF02494408. S2CID 94004320.
- ^ «Тұрақты фтор (ICSC: 0860)». CDC: Халықаралық химиялық қауіпсіздік карталары. Алынған 11 наурыз, 2014.
- ^ «Флорид-стоматологиялық». WebMD. Алынған 11 наурыз, 2014.

