Ферроцений тетрафтороборат - Ferrocenium tetrafluoroborate
 | |
 | |
 | |
| Атаулар | |
|---|---|
| Басқа атаулар дициклопентадиенил темір тетрафторборат | |
| Идентификаторлар | |
3D моделі (JSmol ) | |
| ChemSpider | |
| ECHA ақпарат картасы | 100.156.161 |
PubChem CID |
|
CompTox бақылау тақтасы (EPA) | |
| |
| Қасиеттері | |
| C10H10BFeF4 | |
| Молярлық масса | 272,84 г / моль |
| Сыртқы түрі | қою көк ұнтақ |
| Еру нүктесі | 178 ° C (352 ° F; 451 K) (ыдырайды) |
| Ерігіштік жылы ацетонитрил | Еритін[дәйексөз қажет ] |
| Қауіпті жағдайлар[1] | |
| Қауіпсіздік туралы ақпарат парағы | Сыртқы MSDS |
| GHS пиктограммалары |  |
| GHS сигнал сөзі | Қауіп |
| H314 | |
| P280, P305 + 351 + 338, P310 | |
| Байланысты қосылыстар | |
Байланысты қосылыстар | Ферроцен |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
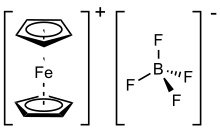
Ферроцений тетрафтороборат болып табылады металлорганикалық қосылыс [Fe (C.) формуласымен5H5)2] BF4. Бұл тұз катионнан тұрады [Fe (C)5H5)2]+ және тетрафторборат анион (BF−
4). Байланысты гексафторофосфат ұқсас қасиеттері бар танымал реагент болып табылады. Катион көбіне Fc деп қысқарады+ немесе Cp2Fe+. Тұздың түсі қою көк және парамагниттік.Ферроцений тұздары кейде бір электронды тотықтырғыш ретінде қолданылады, ал тотықсыздандырылған өнім, ферроцен, инертті және иондық өнімдерден оңай бөлінеді. Ферроцен-ферроцений жұбы электрохимияда сілтеме ретінде жиі қолданылады. Ферроцен-ферроценийдің стандартты потенциалы қалыпты сутегі электродына (NHE) қарсы 0,400 В құрайды.[2] және әр түрлі еріткіштер арасында инвариантты болып саналады.
Дайындық
Сатылымда қол жетімді бұл қосылысты ферроценді қышқылдандыру арқылы, әдетте, темір тұздарымен, содан кейін оны қосу арқылы дайындауға болады фторбор қышқылы.[3] Әр түрлі басқа тотықтырғыштар да жақсы жұмыс істейді, мысалы нитрозил тетрафтороборат.[4] Көптеген ұқсас ферроцений тұздары белгілі.[5]
Пайдаланылған әдебиеттер
- ^ «Ferrocenium tetrafluoroborate 482358». Сигма-Олдрич.
- ^ Бард, А.Ж .; Парсонс, Р .; Джордан, Дж. (1985). Судағы ерітіндідегі стандартты потенциалдар. Нью-Йорк: IUPAC.
- ^ Коннелли, Н.Г .; Geiger, W. E. (1996). «Органометалл химиясына арналған тотықсыздандырғыш химиялық заттар». Хим. Аян 96 (2): 877–910. дои:10.1021 / cr940053x. PMID 11848774.
- ^ Нильсон, Роджер М .; Макманис, Джордж Э .; Саффорд, Ланс Л .; Уивер, Майкл Дж. (1989). «Ферроцений-ферроценнің өзін-өзі алмастыру кинетикасына еріткіш пен электролиттің әсері. Қайта бағалау». J. физ. Хим. 93 (5): 2152. дои:10.1021 / j100342a086.
- ^ Ле-Брас, Дж .; Цзяо, Х .; Мейер, В. Хэмпель, Ф .; Gladysz, J. A. (2000). «17 валентті электронды рений метил кешенінің синтезі, кристалдық құрылымы және реакциялары [(η5-C5Мен5) Қайта (NO) (P (4-C)6H4CH3)3) (CH3)]+ B (3,5-C)
6H
3(CF
3)
2)−
4: 18-электронды метил және метилиден кешендерімен байланыстыруды эксперименттік және есептеуді салыстыру ». J. Organomet. Хим. 616: 54–66. дои:10.1016 / S0022-328X (00) 00531-3.
